在我们的日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品。这里的碘、铁、钙、硒、氟应理解为
| A.元素 | B.单质 | C.分子 | D.氧化物 |
铅蓄电池在现代生活中具有广泛的应用。已知铅蓄电池的电解质溶液为H2S04溶液,其充电、放电按下式进行:Pb+PbO2+2H2SO4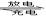 2PbSO4+2H2O,有关该电池的说法正确的是
2PbSO4+2H2O,有关该电池的说法正确的是
| A.充电时化学能转化为电能 |
| B.放电时溶液中的H+向负极移动 |
| C.充电时电池的正极与电源的正极相连 |
| D.放电时负极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42- |
下列实验操作中,错误的是
| A.配制100 g 5%的食盐溶液时,需将5 g食盐放入烧杯中,加95 mL水搅拌溶解即可 |
| B.配制0.1 mol·L-1的硫酸溶液时,将量取的浓硫酸放入容量瓶中加水稀释 |
| C.测定硫酸铜晶体结晶水含量时,需边加热边搅拌,防止晶体飞溅 |
| D.中和热测定实验中,应用环形玻璃搅拌棒轻轻搅动混合液 |
下列关于化工生产原理的叙述中,均符合目前工业生产实际的是
| A.氯碱工业中,电解槽的阳极区产生NaOH |
| B.氯气和氢气混合在光照条件下生成氯化氢,用水吸收得到盐酸 |
| C.合成氨工业中,由于氨易液化,N2、H2循环使用,所以总体上氨的产率很高 |
| D.二氧化硫在接触室被氧化成三氧化硫,三氧化硫在吸收塔内被水吸收制成浓硫酸 |
阿伏加德罗常数的近似值为6.02×1023,下列说法中正确的是
| A.12 g金刚石中所含共价键数目为6.02×1023 |
| B.22.4 L的HCI溶于水,溶液中H+离子数为6.02×1023 |
| C.1 mol CO2与含1 mol NaOH的溶液反应后,溶液中HCO3-离子数为6.02×1023 |
| D.Na2O2与H2O反应,常温常压下生成16 gO2,反应中转移电子数为6.02×1023 |
某苯的同系物分子式为C11H16,经分析分子中除含 外,不再含其他环状结构,还含有两个—CH3、两个—CH2—、一个CH
外,不再含其他环状结构,还含有两个—CH3、两个—CH2—、一个CH ,它可能的结构有()
,它可能的结构有()
| A.4种 | B.5种 | C.6种 | D.7种 |