相同温度下,体积均为0.25L的两个恒容容器中发生可逆反应:X2(g)+3Y2(g) 2XY3(g)
2XY3(g)
ΔH=-92.6 kJ·mol-1,实验测得反应在起始、达到平衡时的有关数据如下表所示:
| 容器编号 |
起始时各物质物质的量/mol |
达平衡时体系能量的变化 |
||
| X2 |
Y2 |
XY3 |
|
|
| ① |
1 |
3 |
0 |
放热46.3 kJ |
| ② |
0.8 |
2.4 |
0.4 |
Q(Q>0) |
下列叙述不正确的是
A.容器①、②中反应达平衡时XY3的平衡浓度相同
B.容器①、②中达到平衡时各物质的百分含量相同
C.达平衡时,两个容器中XY3的物质的量浓度均为2 mol·L-1
D.若容器①体积为0.20 L,则达平衡时放出的热量大于46.3 Kj
下列说法不正确的是
| A.氢能、核能均是无污染的高效能源 |
| B.公共汽车大部分采用天然气作为燃料可减少对大气的污染 |
| C.把煤转化为液态燃料可提高煤的燃烧效率 |
| D.使用催化剂,能增大活化分子百分数,所以反应速率增大 |
下列实验操作完全正确的是
| 编号 |
实验 |
操作 |
| A |
证明SO2有漂白性 |
将SO2气体通入紫色石蕊试液中,观察溶液是否褪色 |
| B |
配制1000mL一定物质的量浓度的硫酸溶液 |
准确称取一定体积浓硫酸,放入到1000mL的容量瓶中,加水稀释,振荡摇匀定容 |
| C |
除去FeC13溶液中混有的FeC12 |
向溶液中通入过量氯水,然后加热煮沸就得到了纯净的FeC13溶液 |
| D |
检验Brˉ的存在 |
在溶液中先加入氯水、在加入CCl4。振荡、静置,观察下层溶液显橙红色 |
把500mLNH4HCO3和Na2CO3的混合溶液分成5等份,取一份加入含amolNaOH的溶液恰好反应完全;另一份加入含bmolHCl的盐酸溶液恰好反应完全,则该混合溶液中c(Na+)为
A.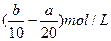 |
B.(2b-a)mol/L |
C.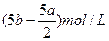 |
D.(10b-5a)mol/L |
现有①NaOH ②Al2(SO4)3③Ba(NO3)2 ④CuSO4 ⑤FeCl3⑥淀粉溶液⑦KI
这7种溶液
| A.不需外加试剂即可鉴别 | B.必须外加试剂才能鉴别 |
| C.如有碘水即能全部鉴别 | D.另有一种溶液即可鉴别 |
下图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强
酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。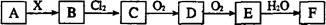
下列说法中不正确的是
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.B和Cl2的反应是氧化还原反应
D.当X是强酸时,C在常温下是气态单质