下列实验操作正确的是:
| 编号 |
实验 |
操作 |
| A |
实验室用自来水制备蒸馏水 |
将自来水倒入烧杯中,小心给烧杯加热 |
| B |
配制一定浓度的氯化钾溶液100mL |
将称好的氯化钾固体放入100 mL容量瓶中,加水溶解,振荡摇匀,定容 |
| C |
检验溶液中是否含SO42- |
先加入稀盐酸,无明显现象,再加入BaCl2溶液 |
| D |
取出分液漏斗中的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
下列各组反应,最终一定能得到白色沉淀的是
| A.向Na2CO3溶液加入CaCl2溶液 |
| B.向CuSO4溶液中加入NaOH溶液 |
| C.向FeCl2溶液中加入过量NaOH溶液 |
| D.向Al2(SO4)3溶液中加入过量NaOH溶液 |
下列物质放置在空气中变质,不是因为发生氧化还原反应而变质的是
| A.Na | B.Na2O2 | C.Na2O | D.FeCl2 |
下列关于铁及其化合物的说法中正确的是
| A.Fe3O4是一种红棕色粉末,俗称磁性氧化铁 |
| B.铁与水蒸气在高温下的反应产物为Fe2O3和H2 |
| C.去除FeCl2溶液中的FeCl3杂质,可以向溶液中加入过量铁粉,然后过滤 |
| D.Fe3+与KSCN反应产生红色沉淀 |
在5mL 0.05 mo1/L的某金属氯化物溶液中,滴加7.5 mL 0.1 mo1/L AgNO3溶液恰好完全反应,则该氯化物中金属元素的化合价为
| A.+1 | B.+2 | C.+3 | D.+4 |
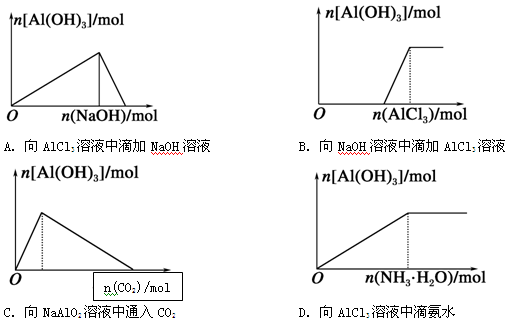
下列有关Al(OH)3的图像不正确的是