已知299 K时,合成氨反应 N2 (g ) + 3H2 ( g ) 2NH3 ( g ) △H =" -92.0" kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
2NH3 ( g ) △H =" -92.0" kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
| A.一定大于92.0 kJ | B.一定等于92.0 kJ |
| C.一定小于92.0 kJ | D.不能确定 |
下列反应一定能自发进行的是()
| A.放热反应 | B.熵增加的反应 | C.熵增加的吸热反应 | D.熵增加的放热反应 |
某温度下在容积为2 L的密闭容器中,发生2X(g)+Y(g) 2W(g)的反应,当充入1 mol X和1 mol Y,经20 s达到平衡时生成了0.4 mol W。下列说法正确的是
2W(g)的反应,当充入1 mol X和1 mol Y,经20 s达到平衡时生成了0.4 mol W。下列说法正确的是
| A.若升高温度,W的体积分数减小,则该反应ΔH<0 |
| B.以Y的浓度变化表示的反应速率为0.01 mol/(L·s) |
| C.在其他条件不变的情况下,增加1 mol X,则X和Y的转化率均提高 |
| D.增大压强正反应速率增大,逆反应速率减小,则平衡向正反应方向移动 |
在密闭容器中,反应X2(g)+Y2(g) 2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是
2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是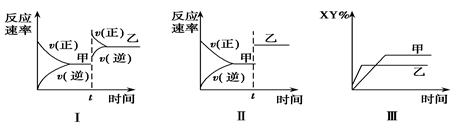
| A.图Ⅰ是增大压强的变化情况 |
| B.图Ⅱ是一定是加入催化剂的变化情况 |
| C.图Ⅲ是增大压强或升高温度的变化情况 |
| D.图Ⅲ一定是升高温度的变化情况 |
反应N2(g)+3H2(g) 2NH3(g) ΔH<0,在某一时间段中反应速率与反应过程的曲线如下图所示,则NH3的百分含量最低的一段时间是
2NH3(g) ΔH<0,在某一时间段中反应速率与反应过程的曲线如下图所示,则NH3的百分含量最低的一段时间是
| A.t0~t1 | B.t2~t3 | C.t3~t4 | D.t5~t6 |
对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列有关叙述正确的是
①生成物的百分含量一定增加 ②生成物的产量一定增加
③反应物的转化率一定增大 ④反应物的浓度一定降低
⑤正反应速率一定大于逆反应速率 ⑥使用了适宜的催化剂
| A.②⑤ | B.①② | C.③⑤ | D.④⑥ |