已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,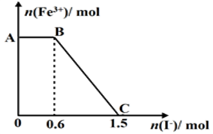
下列说法中不正确的是
| A.图中AB段的氧化剂为K2Cr2O7 |
| B.图中BC段发生的反应为2Fe3++2I- =2Fe2++I2 |
| C.开始加入的K2Cr2O7为0.25 mol |
| D.K2Cr2O7可与FeSO4反应的物质的量为1:3。 |
如果家里的食用油混有水份,你将采用下列何种方法分离()
| A.过滤 | B.蒸馏 | C.分液 | D.萃取 |
下列说法正确的是()
| A.我国居民食用的碘盐添加的是碘单质 |
| B.使用青霉素时,直接静脉注射可以不用进行皮肤敏感试验 |
| C.阿司匹林有防止心脏病发作以及提高免疫功能的作用,可以经常吃 |
| D.味精可以增加食物的鲜味,但摄入过多对人体有害 |
以下气体因与人体的血红蛋白作用而引起中毒的是()
| A.Cl2 | B.SO2 | C.H2S | D.CO |
下列饮食习惯科学的是()
| A.多吃肉,少吃蔬菜水果 |
| B.合理摄入糖类、油脂等,注意膳食平衡 |
| C.为防止变胖,炒菜时不放油 |
| D.多饮用纯净水,少饮用矿泉水 |
坏血病患者应该多吃的食物是()
| A.水果和蔬菜 | B.鱼肉和猪肉 | C.鸡蛋和鸭蛋 | D.糙米和肝脏 |