某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42—、CO32—等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示,下列说法正确的是
| A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+ |
| B.原溶液中含有的Fe3+和Al3+的物质的量之比为1∶1 |
| C.原溶液中一定含有SO42—和Na+ |
| D.反应最后形成的溶液中溶质只有Na2SO4 |
下列图示与对应的叙述一定正确的是()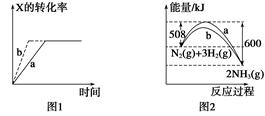
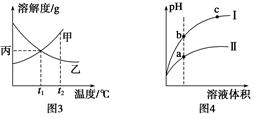
A.图1所示,反应:X(g)+2Y(g)  3Z(g),b的压强一定比a大 3Z(g),b的压强一定比a大 |
| B.图2表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 |
| C.图3所示,t1℃时质量分数均为20%的甲、乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 |
| D.图4所示,用水稀释pH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a |
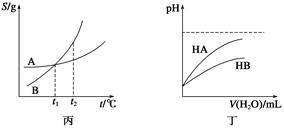
关于下列各图的叙述,正确的是()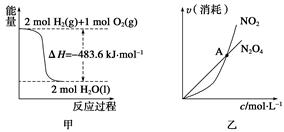
A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6 kJ·mol-1
B.乙表示恒温恒容条件下发生的可逆反应2NO2(g)  N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液的pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
在由水电离的c(H+)=10-14 mol·L-1的溶液中,一定能大量共存的离子组是( )
| A.K+、Fe2+、S、MnO4— |
| B.Na+、Cl-、NO3—、SO42— |
| C.Al3+、NO3—、Cl-、SO42— |
| D.Na+、AlO2—、Br-、Cl- |
室温下,某溶液中水电离出的H+和OH-的物质的量浓度乘积为1×10-26,该溶液中一定不能大量存在的是( )
| A.Cl- | B.HCO3— | C.Na+ | D.NO3— |
已知25 ℃时KW=10-14,如果100 ℃时KW=5.5×10-13,这说明( )
| A.100 ℃时水的电离程度较小 |
| B.前者c(H+)较后者大 |
| C.水的电离过程是一个吸热过程 |
| D.100 ℃时0.1 mol·L-1 DCl的重水溶液中水的电离程度一定是室温时电离程度的10倍 |