【化学——选修3:物质结构与性质】
(1)含碳物质不完全燃烧会产生CO。血红蛋白中含有Fe2+,CO易与血红蛋白结合成稳定的配合物而使人中毒,写出铁离子(Fe3+)的核外电子排布式为 ,CO有多种等电子体,其中常见的一种分子是 。利用CO可以合成化工原料COCl2、配合物Fe(CO)5等,已知一个COCl2分子中每个原子最外层都形成8电子的稳定结构,则一个COCl2分子内含有 个δ键,C原子的杂化方式为 。Fe(CO)5等在一定条件下分解生成CO和铁,反应过程中断裂的化学键是 ,形成的化学键是 。
(2)A、B均为短周期金属元素。依据下表数据,回答问题:
| 电离能/kJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
| A |
932 |
1 821 |
15 390 |
21 771 |
| B |
738 |
1 451 |
7 733 |
10 540 |
写出A原子的电子排布图 ,Al原子的第一电离能 (填:“大于”、“小于”或“等于”)738 kJ·mol-1,原因是 。
(3)下图是一种镍(Ni)镧(La)合金储氢后的晶胞结构图。该合金储氢后,含0.5mol Ni的合金可吸附氢气的体积(标况)为 。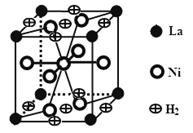
已知:①向KMnO4晶体中滴加浓盐酸,产生黄绿色气体;
②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;
③取少量实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。
下列判断正确的是 ( )
| A.上述实验证明氧化性:KMnO4>Cl2>Fe3+>I2 |
| B.上述实验中,共有两个氧化还原反应 |
| C.实验①生成的气体通入紫色石蕊试液中,溶液只有变红的现象 |
| D.实验②证明Fe2+既有氧化性又有还原性 |
下列结论错误的是()
①微粒半径:K+>Al3+>S2->C1-
②氢化物的稳定性:HF>HC1>H2S>PH3>SiH4
③离子的还原性:S2->C1->Br->I-④氧化性:C12>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K
| A.只有① | B.①③ | C.②④⑤⑥⑦ | D.①③⑤ |
已知原子序数,可能推断原子的( )
①质子数②中子数③质量数④核电荷数⑤核外电子数⑥原子结构示意图
⑦元素在周期表中的位置
| A.①②③④⑥ | B.①④⑤⑥⑦ | C.②③④⑤⑦ | D.③④⑤⑥⑦ |
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如下图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是 ( )
A.OH -+HCl ="==" H2O+Cl-
B.Ca(OH)2+Cu2+ ="==" Ca2++Cu(OH)2
C.Fe+Cu2+ ="==" Cu+Fe2+
D.Fe+2H+ ="==" Fe3++H2↑
下列说法正确的是( )
| A.含有离子键的化合物一定是离子化合物 |
| B.含有共价键的化合物一定是共价化合物 |
| C.所有物质都含有共价键 |
| D.均由非金属元素形成的化合物不可能是离子化合物 |