NA表示阿伏加德罗常数,下列计算关系正确的是
| A.体积均为22.4L的N2和CO,所含分子数均为NA |
| B.1.7g H2O2中含有的电子数为0.9 NA |
| C.标准状况下,11.2L CCl4含有的分子数为0.5NA |
| D.含有NA个氦原子的氦气在标准状况下的体积约为11.2L |
设NA为阿伏加德罗常数的值,下列有关说法不正确的是
| A.标准状况下,48gO3含有的氧原子数是3NA |
| B.含107g Fe(OH)3的胶体中胶粒总数是NA |
| C.0.5L0.2mol·L-1的NaCl溶液中含有的Na+是0.1NA |
| D.标准状况下,33.6LCO中含有的原子数是3NA |
下列实验操作中正确的是
| A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B.蒸馏操作时,应向蒸馏液体中加入几块沸石,以防止暴沸 |
| C.分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出 |
| D.萃取操作时,可以选用CCl4或酒精作为萃取剂从碘水中萃取碘 |
科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2相同的是
| A.原子数 | B.分子数 | C.体 积 积 |
D.物质的量 |
若以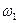 和
和 分别表示浓度为
分别表示浓度为 和
和 氨水的质量分数,且知2a=b,则下列推断正确的是(已知氨水的密度比纯水的小)( )
氨水的质量分数,且知2a=b,则下列推断正确的是(已知氨水的密度比纯水的小)( )
A. |
B.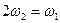 |
C. |
D.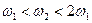 |
对于溶液中发生的离子反应,下列说法正确的是(  )
)
①不可能是氧化还原反应 ②只能是复分解反应 ③可能是置换反应 ④不能有分子参加
| A.①③ | B.③ | C.①② | D.③④ |