5种固体物质A、B、C、D、E由下表中不同的阴阳离子组成,它们均易溶于水。

分别取它们的水溶液进行实验,结果如下:
①A溶液与C溶液混合后产生蓝色沉淀,向该沉淀中加入足量稀HNO3,沉淀部分溶解,剩余白色固体;
②B溶液与E溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④B溶液与D溶液混合后无现象;
⑤将38.4 g Cu片投入装有足量D溶液的试管中,Cu片不溶解,再滴加1.6 mol·L-1稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现。
(1)据此推断A、C的化学式为:A ;C 。
(2)写出步骤②中发生反应的化学方程式 。
(3)D溶液中滴入石蕊试液,现象是 ,
原因是 (用离子方程式说明)。
(4)步骤⑤中若要将Cu片完全溶解,至少加入稀H2SO4的体积是 mL。
(5)现用500 mL 3 mol·L-1的E溶液充分吸收11.2 L CO2气体(标准状况下),反应后溶液中各离子的物质量浓度由小到大的顺序为 。
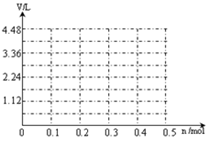
(6)若用惰性电极电解A和B的混合溶液,溶质的物质的量均为0.1 mol,请在坐标系中画出通电后阳极产生气体的体积(标准状况下)V与通过电子的物质的量n的关系(不考虑气体溶于水)。
 ’
’
A、B、C、D、E、F的原子序数依次增大,它们都具有相同的核外电子层数。已知:A、C、F三种原子最外层共有11个电子,且这三种元素原子的最高价氧化物对应水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素的符号:A ,B ,E 。
(2)把B的单质(片状)放入滴有酚酞的沸水中,观察到的现象是 ,反应的化学方程式是 。
(3)A、C两种元素的最高价氧化物对应水化物反应的离子方程式是 。
有四种化合物W、X、Y、Z,它们都是由短周期元素A、B、C、D、E中的两种元素组成的。已知:
(a)A、B、C、D、E五种元素的原子序数依次增大,且A、D同主族,C、E同主族,B、C同周期。
(b)W由A、B组成,分子中原子个数比为A∶B=1∶1,常温时为气态。
(c)X由A、C组成,分子中原子个数比为A∶B=2∶1,常温时为液态。
(d)Y是由C、D形成的离子化合物,且Y中相应元素的微粒之比为:C∶D=1∶1。
(e)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阴、阳离子个数比为1∶2。试完成下列各小题:
(1)各元素符号:A_____,B_____,C_____,D_____,E_____。
(2)W的化学式:__________。
(3)X的结构式:__________。
(4)Y的电子式:__________。
(5)Z的化学式:__________。
(6)写出下列反应化学方程式:Y与水反应__________。
A、B、C、D是四种短周期主族元素,其中B的原子序数最小,A、B同主族,C、D同主族,A比C的核外少两个电子;D元素一种原子的质量数是其质子数的两倍多2,又是该原子最外层电子数的3倍。判断A、B、C、D各是什么元素,并比较A、B、C三种元素的最高价氧化物对应的水化物溶液酸、碱性的相对强弱。
(1)A_____、B_____、C_____、D_____。(填元素符号)
(2) _____ (填酸性或碱性):_____>_____>_____。(填分子式)
A、B两元素,A的原子序数为x,A和B所在周期包含元素种类数目分别为m和n。如果A和B同在ⅠA族,当B在A的上周期时,B的原子序数为_____;当B在A的下一周期时,B的原子序数为_____;如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为_____;当B在A的下一周期时,B的原子序数为_____。若A的氯化物化学式为ACly,分子中各原子最外层电子数之和为26,则y的值为_____。
在水溶液中, 和S2-发生反应的离子方程式如下:
和S2-发生反应的离子方程式如下: +3S2-+6H+
+3S2-+6H+  Y-+3S↓+3H2O
Y-+3S↓+3H2O
(1) 中Y元素的化合价是。
中Y元素的化合价是。
(2)Y元素原子的最外层电子数是。
(3)比较S2-和Y-的还原性。