()卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多卤代甲烷常作为有机溶剂,其中分子结构为正四面体的是 _________ .工业上分离这些多氯代甲烷的方法是 _________ .
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构简式_________ (不考虑立体异构).
(3)聚氯乙烯是生活中常用的塑料.工业生产聚氯乙烯的一种工艺路线如下:
反应①的化学方程式为 _________ ,反应类型为 _________ ;反应②的反应类型为 _________ .
海藻中提取碘的流程如图:
(1)指出提取碘的过程中有关实验操作③的名称:▲;
写出过程②中有关反应的离子方程式▲。
(2)在3mL碘水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是
▲。(注:下图试管中深色区为紫红色溶液)
(3)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出下图实验装置
中的错误之处。(加热装置烧杯下已垫石棉网)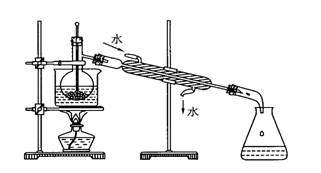
①▲;
②▲。
实验室欲配制90mL浓度为1.00mol·L-1的Na2CO3溶液:
(1)配制时的实验步骤为:计算、称量、溶解、转移(洗涤)、▲、摇匀;
(2)本实验中必须用到的仪器有托盘天平、药匙、玻璃棒、烧杯、量筒、胶头滴管、
▲(注明所需仪器的规格)。
(3)某同学欲称量Na2CO3的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为▲g,要完成本实验该同学应称出▲g Na2CO3。
(4)使用容量瓶前必须进行的一步操作是▲。
(5)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)
①没有洗涤烧杯和玻璃棒▲ ;②容量瓶不干燥,含有少量蒸馏水▲ ;
甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验。
(1)甲组:沉淀分析法:
把一定量的混合物溶解后加入过量CaCl2,然后将所得沉淀过滤、洗涤、烘干、称量。确定CaCl2溶液是否过量的方法是洗涤沉淀并判断沉淀是否洗净的操作是_______________________________________。
(2)乙组:气体分析法:
把一定量的混合物与足量盐酸反应后,用如图装置测定产生的CO2气体的体积,为减小CO2的溶解,B中溶液应是____________,选用该溶液后实验结果还是不准确,原因是_________________。
(3)请你设计一个与甲、乙两组操作不同的实验方案,测定混合
物中Na2CO3的含量。
方法:;
试剂:_________________________________________________________________。
用到的玻璃仪器:_______________________________________________(至少2件)。
某研究性学习小组成员,利用稀硫酸与某金属的反应来探究影响化学反应速率的因素,下表是研究过程中记录的实验数据(表中某些数据记录已模糊不清,个别数据已丢失)。若实验操作、数据记录均是正确的,试分析上述数据回答下列问题:
(1)该实验主要是探究___________、和对反应速率的影响。
(2)经仔细辨认,模糊的数据疑为25、50、125、250,试将这些疑似数据填入表中,使实验数据较为合理。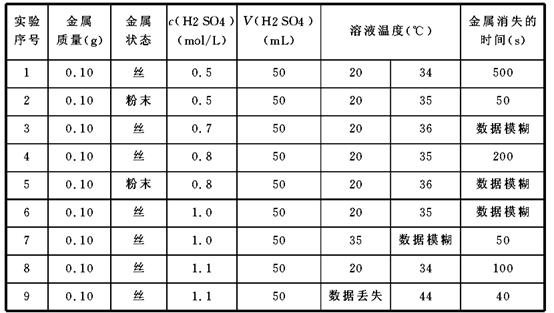
工业碳酸钠由于在生产过程中原料盐和工艺等的原因,常会含有Na2SO4、NaCl中的一种或两种杂质。现有工业碳酸钠样品,某化学兴趣小组就工业碳酸钠中是否含有这两种杂质进行探究。
实验室有以下的仪器和药品可供使用:
烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹
1.0mol·L-1 H2SO4溶液,1.0mol·L-1HNO3溶液,1.0mol·L-1 HCl溶液, 1.0mol·L-1 NaOH溶液, 0.1mol·L-1 AgNO3溶液,0.1mol·L-1 BaCl2溶液, 0.1mol·L-1 Ba(NO3)2溶液,蒸馏水
以下是部分实验探究过程:
⑴提出假设:根据题意,工业碳酸钠中含有杂质有种可能的情况。
⑵设计实验方案,进行实验,写出实验操作步骤,预期的现象和涉及反应的离子方程式
| 编号 |
实验操作 |
预期现象 |
相关离子方程式 |
| ① |
|||
| ② |
|||
| ③ |