已知:①SO2 + 2NaOH = Na2SO3+H2O;②SO2 + 2H2S ="3S↓+" 2H2O;
③SO2+Cl2+2H2O=H2SO4+2HCl
(1)请用上述三个反应中的物质填下表:
| 类型 |
酸性氧化物 |
含氧酸 |
碱 |
含氧酸盐 |
| 化学式 |
|
|
|
|
(2)属于氧化还原反应的有 (填序号);分离②反应中的产物,实验操作是 ;③反应中SO2的作用 (填“氧化剂”或“还原剂”)。
(3)检验③中产物的阴离子,请完成表格中的方案: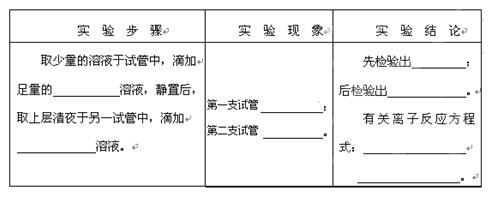
冶炼金属一般有下列方法:①焦炭法,②水煤气(或氢气,或一氧化碳)法,③活泼金属置换法,④电解法;四种方法在工业上均有运用。
(1)孔雀石[Cu2(OH)2CO3],光卤石(KCl·MgCl2·6H2O)。请对下表中的金属冶炼方法进行分析,从上述四种方法中选择相应的序号填入表中空格:
| 火烧孔雀石炼铜 |
湿法炼铜 |
铝热法炼铬 |
从光卤石中炼镁 |
火烧孔雀石炼铜所发生反应的化学方程式(写主要的两个):
;
。
(2)请再举出使用上述方法冶炼金属的例子各一个(用化学方程式表示):
②;
③;
④。
和
是具有相同碳原子数的一氯代物,
-
转换关系如图所示:
根据框图回答下列问题;
(1)
的结构简式是;
(2)反应③的化学方程式是;
(3)上述转换中属于取代反应的是;(填写反应序号)
(4)图中与
互为同分异构体的是;(填化合物代号)。图中化合物带有的含氧官能团有种。
(5)
在硫酸催化下与水反应的化学方程式是;
(6)
的结构简式是;名称是。
有一白色固体混合物,可能含有有的阴、阳离子分别是
| 阳离子 |
K+Ba2+Ag+Mg2+NH4+ Na+ |
| 阴离子 |
SO42-SO32-CO32-AlO2- |
为了鉴定其中的离子,现进行如下实验,根据实验现象,填写下列表格:
(1)取该粉末,加水后得到无色溶液,且未嗅到气味;用pH试纸测得溶液的pH为12。
| 排除的离子 |
排除的依据 |
(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出。
| 肯定存在的离子 |
判断依据 |
| 排除的离子 |
排除的依据 |
(3)尚待检验的离子及其检验方法
| 尚待检验的离子 |
检验方法 |
下图中
~
均代表无机物或其水溶液,其中
、
、
是单质,
是地壳中含量最高的金属元素,
是气体,
是磁性材料。
根据图示回答问题:
(1)写出下列物质的化学式:
,E,I;
(2)反应①的化学方程式是;
反应②的化学方程式是;
(3)
与盐酸反应的化学方程式是;
反应后的溶液与
反应的化学方程式是。
1
水蒸汽和炽热的焦炭反应生成水煤气,反应吸热131.4
·
。利用该反应生成的氢气和空气中的氮气合成氨,其反应的
<0。氨可以用于制备硝酸。请回答:
(1)生成水煤气的热化学方程式是;
(2)合成氨需要在较大的压力下进行的原因是;
(3)温度过高或过低对合成氨的影响是;
(4)由氨生成
的各步反应的化学方程式是;
(5)某化肥厂由
制备
,进而生产硝铵(NH4NO3)。假设由氨氧化生成
的总产率是85%,而
和
完全反应生成
。列式计算:
①从
制取
过程中,用于中和硝酸所需的氨占总的氨消耗量的分数;
②若氨的消耗总量为100
,可生产
的量。