关于25℃时,pH = 12的NaOH溶液,下列说法错误的是
| A.c(OH-) =c(Na+) + c(H+) |
| B.由水电离出的c(OH-) = 1.0×10-12 mol·L-1 |
| C.与等体积pH = 2的醋酸混合后所得溶液显碱性 |
| D.与等体积0.01 mol·L-1氯化铵溶液混合后所得溶液中:c(Na+)> c(NH4+) |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=" +" 49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9 kJ·mol-1
下列说法正确的是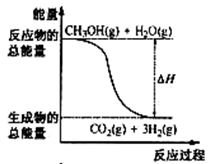
| A.CH3OH的燃烧热为192.9 kJ·mol-1 |
| B.反应①中的能量变化如上图所示 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
| D.根据②推知反应:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) 的△H>-192.9kJ·mol-1 |
Cl2可用来消灭田鼠,使用时可将Cl2通过管子灌入洞中,这是利用Cl2下列性质中的
| A.黄绿色 | B.密度比空气大 |
| C.有毒 | D.较易液化 |
巴豆酸的结构简式为 CH3—CH="CH—COOH" ,现有
①氯化氢
②溴水
③纯碱溶液
④2-丁醇
⑤酸性高锰酸钾溶液
试根据巴豆酸的结构特点,判断在一定的条件下,能与巴豆酸反应的物质是
| A.只有②④⑤ | B.只有①③④ |
| C.只有①②③④ | D.全部 |
同一周期的X、Y、Z三种主族元素,已知其最高价氧化物对应水化物的化学式分别为H2XO3、H3YO4、H2ZO4,下列说法正确的是
| A.气态氢化物的稳定性:XH4>YH3>H2Z; |
| B.元素非金属性强弱关系:X>Y>Z |
| C.最高价氧化物对应水化物酸性:H2XO3>H3YO4>H2ZO4 |
| D.原子半径:X>Y>Z |
从海水提取溴的过程中,吸收塔内溴蒸气和吸收剂SO2发生的化学反应为Br2 + SO2 + 2H2O ="=" 2HBr + H2SO4,下列说法正确的是
| A.Br2在反应中表现氧化性 | B.SO2在反应中被还原 |
| C.Br2在反应中失去电子 | D.1mol氧化剂在反应中得到2mol电子 |