从矿物学资料查得,一定条件下自然界存在如下反应: 14CuSO4+5FeS2+12H2O = 7Cu2S+5FeSO4+12H2SO4下列说法正确的是
| A.Cu2S是还原产物,反应中1 mol CuSO4失1 mol电子 |
| B.5 mol FeS2发生反应,有10 mol电子转移 |
| C.产物中的SO42-离子有一部分是氧化产物 |
| D.FeS2只作还原剂 |
在密闭容器中,一定条件下进行反应:mA(气)+nB(气)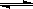 pC(气)+qD(气),若增大压强,或升高温度,重新达到平衡,
pC(气)+qD(气),若增大压强,或升高温度,重新达到平衡,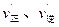 随时间化过程均如图所示,则对该反应叙述正确的是()
随时间化过程均如图所示,则对该反应叙述正确的是()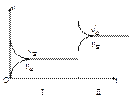
| A.正反应是放热反应,m+n < p+q |
| B.逆反应是放热反应,m+n > p+q |
| C.正反应是放热反应,m+n > p+q |
| D.逆反应是放热反应,m+n < p+q |
当2SO2+O2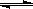 2SO3 达到平衡后,通入
2SO3 达到平衡后,通入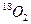 一定时间后,
一定时间后,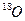 存在于()
存在于()
| A.SO3、O2 | B.SO2、SO3 | C.SO2、SO3、O2 | D.SO2、O2 |
将气体A、B置于容积为2 L的密闭容器中,发生如下反应:
4A(g)十B(g)=2C(g)
反应进行到4 s末,测得A为0.5 mol,B为0.4 mol,C为0.2 mol。则用反应物A浓度的减少来表示该反应的速率应为()
A. 0.025 mol/(L·s) B. 0.012 5 mol/(L·s)
C. 0.05 mol/(L·s) D. 0.1 mol/(L·s)
“嫦娥奔月”是一个充满浪漫主义的中国神话故事。2007年10月24日我国“嫦娥一号”探月卫星由长三甲火箭送入预定的轨道。长三甲火箭第三级推进剂采用低温液氧/液氢。已知在298K时,2g氢气与氧气完全反应生成液态水放热285.8kJ,则此反应的热化学方程式为()
| A.2H2(g) + O2(g) ="==" 2H2O(l)△H=-285.8KJ·mol-1 |
| B.2H2(g) + O2(g) ="==" 2H2O(l)△H=+285.8KJ·mol-1 |
| C.H2(g) + 1/2 O2(g) ="==" H2O(l)△H=-285.8KJ·mol-1 |
| D.H2(g) + 1/2 O2(g) ="==" H2O(g)△H=-285.8KJ·mol-1 |
下列微粒不具有的还原性是
| A.S | B.H+ | C.Fe2+ | D. Cl- Cl- |