某温度下重水中存在电离平衡D2O  D+ + OD-,D2O的离子积常数=1.0×10-12,若pD=-lgc(D+),该温度下有关分析正确的是
D+ + OD-,D2O的离子积常数=1.0×10-12,若pD=-lgc(D+),该温度下有关分析正确的是
| A.0.1molNaOD溶于重水制成1L溶液,pD=13 |
| B.将pD=4的DCl的重水溶液稀释100倍,所得溶液pD=6 |
| C.向30mL0.5mol·L-1NaOD的重水溶液中加入20mL0.5mol·L-1DCl的重水溶液,所得溶液pD=13 |
| D.pD=10的NaOD的重水溶液中,由重水电离出的c(OD-)为1×10-10mol·L-1 |
下列四种溶液:①pH=2的CH3COO H
H 溶液;②pH=2的HCl溶液;③pH=12的氨水;
溶液;②pH=2的HCl溶液;③pH=12的氨水;
④pH=12的NaOH溶液。相同条件下,有关上述溶液的比较中,正确的是 ( )
| A.由水电离的c(H+):①=②>③=④ |
| B.将②、③两种溶液混合后,若pH=7,则消耗溶液的体积:②>③ |
| C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| D.向等体积的四种溶液中分别加入100 mL水后,溶液的pH:③>④>①>② |
下列对化学平衡移动的分析中,不正确的是()
①已达平衡的反应C(s)+H2O(g) CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g) 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③有气体参加的反应达平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
| A.①②④ | B.①②③ | C.②③④ | D.①②③④ |
对于可逆反应A(g)+2B(g)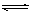 2C(g)(正反应吸热),下列图象中正确的是()
2C(g)(正反应吸热),下列图象中正确的是()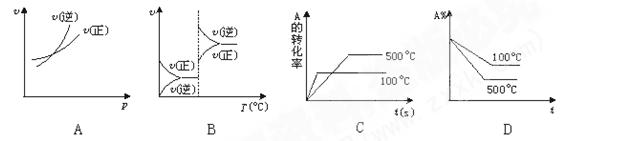
关于用水制取二级能源氢气,以下研究方向正确的是()
| A.构成水的氢和氧都是可以燃烧的物质,因此,可研究在水不分解的情况下,使氢成为二级能源 |
| B.设法将太阳光聚集,产生高温,使水分解产生氢气 |
| C.寻找高效催化剂,使水分解产生氢气,同时释放能量 |
| D.寻找特殊化学物质,用于开发廉价能源,以分解水制取氢气 |
下列叙述正确的是()
| A.物质燃烧都是放热反应 | B.化学反应总是伴随着能量的变化 |
| C.化学反应中需要加热的反应一定是吸收反应 | D.化学反应中放出的热量就是反应热 |