一定条件下,在体积为10 L的密闭容器中,2 mol X和2 mol Y 进行反应:2X(g)+Y(g) Z(g),经2 min达到平衡,生成0.6 mol Z,下列说法正确的是
Z(g),经2 min达到平衡,生成0.6 mol Z,下列说法正确的是
| A.以X浓度变化表示的反应速率为0.001 mol·L-1·s-1 |
| B.将容器体积变为20 L,Z的平衡浓度为原来的1/2 |
| C.若增大压强,则物质Y的转化率减小 |
| D.若升高温度,X的体积分数增大,则该反应的ΔH>0 |
将CH3COOH与CH3COONa以等物质的量混合配制的稀溶液,其pH为4.7。下列说法错误的是()
| A.CH3COOH的电离作用大于CH3COONa的水解作用 |
| B.CH3COONa的水解作用大于CH3COOH的电离作用 |
| C.CH3COOH的存在抑制了CH3COONa的水解 |
| D.CH3COONa的存在抑制了CH3COOH的电离 |
下列物质的水溶液,由于水解而呈碱性的是()
| A.KHCO3 | B.KOH | C.NH4Cl | D.NaHSO4 |
能正确表示下列反应的离子方程式是()
| A.甲酸钠溶液和盐酸反应: HCOO-+H+====HCOOH |
| B.硫化钠的第一步水解: S2-+2H2O  H2S+2OH- H2S+2OH- |
| C.醋酸钡溶液和硫酸反应: Ba2++ 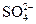 ====BaSO4 ====BaSO4 |
| D.氢氧化钙溶液和碳酸氢镁反应: |
Ca2++OH-+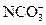 ====CaCO3↓+H2O
====CaCO3↓+H2O
由一价离子组成的四种盐:AC、BD、AD、BC的1mol·L-1溶液,在室温下前两种溶液的pH=7,第三种溶液pH>7,最后一种溶液pH<7,则()
| 碱性 |
酸性 |
|
| A |
AOH>BOH |
HC>HD |
| B |
AOH<BOH |
HC>HD |
| C |
AOH>BOH |
HC<HD |
| D |
AOH<BOH |
HC<HD |
在常温下,纯水中存在电离平衡H2O H++OH-,如要使水的电离程度增大,并使c(H+)增大,应加入的物质是()
H++OH-,如要使水的电离程度增大,并使c(H+)增大,应加入的物质是()
| A.NaHSO4 | B.KAl(SO4)2 | C.NaHCO3 | D.CH3COONa |