下列反应中符合下图图像的是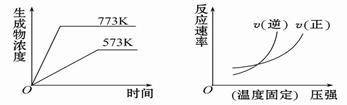
A.N2(g) + 3H2(g)  2NH3(g) ΔH =-Q1 kJ·mol-1 (Q1>0) 2NH3(g) ΔH =-Q1 kJ·mol-1 (Q1>0) |
B.2SO3(g)  2SO2(g) + O2(g) ΔH =" +" Q2 kJ·mol-1 (Q2>0) 2SO2(g) + O2(g) ΔH =" +" Q2 kJ·mol-1 (Q2>0) |
C.4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g) ΔH =-Q3 kJ·mol-1 (Q3>0) 4NO(g) + 6H2O(g) ΔH =-Q3 kJ·mol-1 (Q3>0) |
D.H2(g) + CO(g)  C(s) + H2O(g) ΔH =" +" Q4 kJ·mol-1 (Q4>0) C(s) + H2O(g) ΔH =" +" Q4 kJ·mol-1 (Q4>0) |
固体粉末X中可能含有Fe、Fe2O3、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下: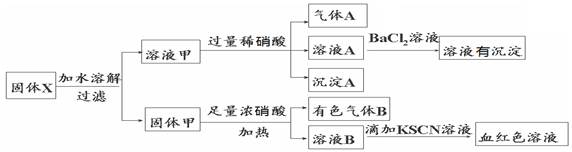
根据上述实验,以下说法正确的是
| A.气体A一定只是NO |
| B.由于在溶液A中加入BaCl2溶液有沉淀产生,因此可以判断溶液中含有K2SO3 |
| C.若向固体甲中加入足量浓盐酸,再加KSCN溶液,没有血红色,则证明原混合物中一定没有Fe2O3 |
| D.溶液甲中一定含有K2SiO3、可能含有KAlO2、MgCl2 |
下列说法正确的是
| A.配制100 mL 1.0 mol/L CuSO4溶液,可将25 g CuSO4·5H20溶于100 mL蒸馏水中 |
| B.将几根火柴头浸于水中,一段时间后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,若出现白色沉淀,说明含有氯元素 |
| C.用纸上层析法分离某些物质时,为了看到色斑,只有有色离子的物质才可以用纸层析法 |
| D.减压过滤时,吸滤瓶内液面高度将达到支管口时,应拔掉吸滤瓶上的橡皮管,并从吸滤瓶支管口倒出溶液 |
如图是甲醇/过氧化氢燃料电池内部结构示意图。 工作时,甲醇和过氧化氢分别进入燃料电池的燃料腔和氧化剂腔,在各自催化剂的作用下发生反应,并向外界输出电能。下列说法不正确的是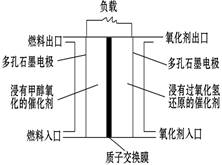
| A.该电池的正极反应式:H2O2+2H++2e—=2H2O |
| B.燃料腔中的多孔石墨电极为该燃料电池的负极,负极产生的H+通过质子交换膜流向正极 |
| C.电池工作时,1 mol甲醇被氧化有6 mol电子转移 |
| D.电路中的电子经正极、负极、质子交换膜后再回到正极,形成闭合回路 |
X、Y、Z、W为短周期元素,原子半径X>Y>Z>W,X、Y、Z处于同一周期,Z、W处于同一主族,X、Y、Z原子序数之和为40,X是短周期中除稀有气体元素外半径最大的元素。下列说法正确的是
| A.若X、Y、W形成的化合物为XYW2,则其水溶液可以显碱性 |
| B.Y的最高价氧化物对应的水化物一定是碱 |
| C.稳定性:W的氢化物>Z的氢化物,沸点:Z的氢化物>W的氢化物 |
| D.X、Y的氧化物晶体类型一定相同 |
下列说法不正确的是
| A.某芳香烃的分子式为C10H14,它不能使溴水褪色,但可使酸性KMnO4溶液褪色,且分子结构中只有一个烷基,符合条件的烃有3种 |
B.将 转化为 转化为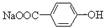 的方法是加入足量的NaOH溶液并加热, 再通入足量的CO2 的方法是加入足量的NaOH溶液并加热, 再通入足量的CO2 |
C.1mol某有机物的结构简式为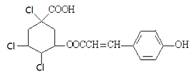 ,通过消去反应脱去1 molHCl时,能得到 5 种不同产物(不考虑立体异构) ,通过消去反应脱去1 molHCl时,能得到 5 种不同产物(不考虑立体异构) |
| D.等质量的甲烷、乙烯、1,3-丁二烯(C4H6)分别充分燃烧,所耗用氧气的量依次减少 |