(10分)使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸。
Ⅰ.实验步骤:
(1)滴定前的准备
①滴定管:___________________→洗涤→润洗→装液→赶气泡→调液面→记录。记录盛装 0.1000 mol/L NaOH溶液的碱式滴定管的初始读数时,液面位置如图所示,则此时的读数为_____________mL。
②锥形瓶:用酸式滴定管量取待测稀盐酸20.00mL于锥形瓶中,向其中滴加2滴酚酞溶液作指示剂。
(2)滴定
用标准的NaOH溶液滴定待测的稀盐酸时,左手操作滴定管活塞,右手旋摇锥形瓶,眼睛注视 。滴定至终点时,记录NaOH溶液的终点读数。再重复滴定3次。
Ⅱ.实验记录:
 滴定次数 滴定次数实验数据/mL |
1 |
2 |
3 |
4 |
| V(样品) |
20.00 |
20.00 |
20.00 |
20.00 |
| V(NaOH)(消耗) |
15.80 |
15.00 |
15.02 |
14.98 |
Ⅲ.数据处理与误差分析:
(1)结合上表数据,计算被测稀盐酸的物质的量浓度是____________mol/L.
(2)在本实验中,下列操作(其他操作正确)会造成测定结果偏低的有______.
A.锥形瓶水洗后未干燥
B.碱式滴定管未用标准NaOH溶液润洗
C.滴定终点读数时俯视读数
D.配制标准液的NaOH固体中混有少量KOH固体
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(13分)某同学设计了如右下图的实验装置来粗略地测定电石中碳化钙的质量分数。
(1)烧瓶中发生反应的化学方程式为____________________________________________;装置B、C的作用是_________________________________,烧瓶要干燥,放入电石后应塞紧橡皮塞,这是为了_________________________________。
(2)所用电石质量不能太大,否则_________________________________,也不能太小,否则 _________________________________;若容器B的容积为250 mL,则所用电石的质量应在___________ g左右(选填:0.03,0.60,1.00,1.50,2.00)。
(3)由分液漏斗往烧瓶里滴加水的操作方法是________________________________。
(4)实验中测得排入量筒中水的体积为V mL、电石的质量为W g,则电石中碳化钙的质量分数是___________%(不计算导管中残留的水,气体中饱和的水蒸气等也忽略不计)。
控制变量法是研究化学变化量的重要思想方法。请仔细观察下表中50mL稀盐酸和1g碳酸钙反应的实验数据:
| 实验 序号 |
碳酸钙 状态 |
C(HCl)/ mol·l-1 |
溶液温度/℃ |
碳酸钙消失 时间/s |
|
| 反应前 |
反应后 |
||||
| 1 |
块状 |
0.5 |
20 |
39 |
400 |
| 2 |
粉末 |
0.5 |
20 |
40 |
60 |
| 3 |
块状 |
0.6 |
20 |
41 |
280 |
| 4 |
粉末 |
0.8 |
20 |
40 |
30 |
| 5 |
块状 |
1.0 |
20 |
40 |
120 |
| 6 |
块状 |
1.0 |
30 |
50 |
40 |
(1)该反应属于反应(填“吸热”或“放热”)。
(2)实验5、6表明对反应速率的影响,说明,反应速率越快。
(3)根据实验1、3、5可以得出条件对反应速率的影响规律是。
(4)从本实验数据中分析,影响化学反应速率的因素还有,能表明这一规律的实验序号是。
已知氯气和氢氧化钠的反应条件不同,产物也不同,在实验室里可用如图所示装置制取氯酸钠次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15mL30%NaOH溶液,并置于热水浴中;
③的试管里盛有15mL8%NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过_________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_________(填写下列编号字母)的净化装置。
| A.碱石灰 | B.饱和食盐水 | C.浓硫酸 | D.饱和碳酸氢钠溶液 |
(2)比较制取氯酸钠和次氯酸钠的条件,指出二者的差异:______________________。
(3)本实验中制取次氯酸钠的离子方程式是__________________________________。
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
| 实验现象 |
原因 |
| 溶液最初从紫色逐渐变为_______色 |
氯气与水反应生成的 使石蕊变色 使石蕊变色 |
| 随后溶液逐渐变为无色 |
|
| 然后溶液从无色逐渐变为_______色 |
(12分)乙二酸(HOOC-COOH)俗称草酸,该酸广泛存在于多种植物的细胞膜内,其晶体通常含有结晶水(H2C2O4·2H2O),晶体的熔点为101.5℃,无水草酸的熔点为189.5℃。草酸易升华,其在157℃时大量升华,并开始分解,分解产物为CO、CO2、H2O。
某研究性学习小组的同学决定对草酸的分解反应进行探究,设计出如下实验验证乙二酸的分解并测定其分解率,操作步骤如下:
①先把乙二酸晶体放在烘箱中进行烘烤,去掉结晶水,备用。
②按图2连接好装置。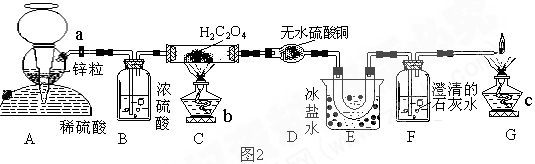
③检查装置的气密性。
④打开活塞a,通入H2一会儿,再关闭a;点然酒精灯b、c。
⑤当C装置中固体消失后,停止加热
⑥打开活塞a,继续通入H2,直至冷却。
试回答下列问题:
⑴检验该套装置的气密性的方法是____________________________________________。
⑵装置A的作用______________________________,B的作用_____________________;
装置E的作用_____________________________。
⑶若分解结束后,不再通入氢气,会使所测的乙二酸的分解率_________(填“增大”、“减小”或“不变”)。
⑷若称取H2C2O4(烘干)的质量为4.5g,实验结束后,称得D、E、F分别增重0.95g、0.40g、1.98g,则乙二酸的分解率为_______________。[
某化学课外小组为了探究CaCl2溶液和Na2SO4溶液反应有没有限度,设计了如下活动过程,请完成表中空格:(已知CaSO4在水中微溶,CaCO3在水中难溶)
| 实验步骤 |
向3—4 mL 1 mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全 |
| 实验现象 |
产生白色沉淀 |
| 离子方程式 |
(1) |
| 小组讨论交流 |
向上述反应后的清液中滴入适量1mol/L的Na2CO3溶液会出现什么现象 |
| 假设出现的实验现象,说明理由 |
假设:Ⅰ无现象 理由:反应没有限度,Ca2+沉淀完全 假设:Ⅱ(2),理由:(3) |
| 证明你的假设 |
现象:产生大量的白色沉淀 |
| 离子方程式 |
(4) |
| 解释出现假设Ⅱ现象的原因 |
(5) |