(6分)(1)有四种一元酸HA、HB、HC、HD,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质的量浓度的HB、HC用同样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为 。
(2)NO2可用氨水吸收生产硝酸铵,25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是 (用离子方程式表示)。向该溶液中滴加bL氨水后溶液显中性,则滴加氨水的过程中水的电离平衡将会 (填“正向”、“逆向”或“不”) 移动,所滴加氨水的浓度为 mol/L。(已知氨水的电离平衡常数Kb=2×10-5)
为了测定某有机物A的结构,做如下实验:
①将3.1 g该有机物完全燃烧,生成0.1 mol CO2和2.7 g水;
②用质谱仪测定其相对分子质量,得如图所示的质谱图;
③其核磁共振氢谱如图
试回答下列问题:
(1)有机物A的相对分子质量是____________。
(2)有机物A的实验式是_______________。
(3)有机物的结构简式为___________________
(4)若以分子量为28的某烃为原料合成机物A,则所经过的反应类型为_______________
(填反应名称用→连接)
根据下面的反应路线及所给信息填空。
(1)A的结构简式是_________________
(2)①的反应类型是________________,③的反应类型是________。
(3)反应③的化学方程式是:___________________________________________。
(4)反应④的化学方程式是:___________________________________________。
(1)在下面元素周期表中全部是金属元素的区域为。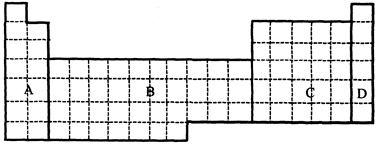
(a)A (b)B (c)C (d)D
(2)短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子数的2倍;Y元素单质为双原子分子,其氢化物水溶液呈碱性;1mol单质Z跟盐酸完全反应,能置换出22.4L的H2(标准状况);W元素原子核外M层电子数目比K层多1个;
①请写出元素X的一种核素的化学符号;
②写出元素Y在周期表中的位置;
③Z、W两元素相比较,金属性较强的元素是(填元素符号),可以验证该结论的实验是。
(a)比较两种元素单质的熔点
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)比较这两种元素的最高价氧化物对应水化物的碱性
(d)比较这两种元素的气态氢化物的稳定性
图表法是常用的科学研究方法,下表列出了同周期的四种短周期元素的部分性质(“电负性”即元素对应原子吸引电子能力的标度):
| 元素编号 |
A |
B |
C |
D |
E |
| 电负性 |
3.0 |
2.5 |
X[ |
1.5 |
0.9 |
| 原子半径(单位nm) |
0.099 |
0.102 |
0.110 |
0.143 |
0.186 |
| 主要化合价 |
-1,+7 |
-2,+6 |
-3,+5 |
+3 |
+1 |
请回答下列问题:
(1)写出E元素的离子结构示意图;
(2)X的值应为(填字母);
A.3.6 B.3.1 C.2.1 D.1.4
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系;
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是:(用化学式表示)
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:
(6)D、E最高价氧化物对应水化物相互反应的离子方程式:
下列六种物质中①Ar ②CO2 ③NH4Cl ④KOH ⑤Na2O2 ⑥MgCl2请回答:
(1)只存在共价键的是;(填写序号)
只存在离子键的是;(填写序号)
不存在化学键的是 。(填写序号)
(2)Na2O2的电子式为;
(3)KOH溶于水,破坏了;氯化铵受热分解破坏了。