(15分)资源化利用CO2不仅可以减少温室气体的排放,还可以重新获得燃料或重要工业产品。
(1)有科学家提出可利用FeO吸收和利用CO2,相关热化学方程式为:6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) △H=-76.0kJ/mol,该反应中每生成1mol Fe3O4,转移电子的数目为 。
(2)在一定条件下,二氧化碳转化为甲烷的反应为:CO2(g)+4H2(g)  CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0
①向一容积为2L的恒容密闭容器中充入一定量的CO2和H2,在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2 0.2mol/L, H2 0.8 mol/L, CH4 0.8 mol/L, H2O 1.6 mol/L。起始充入CO2和H2的物质的量分别为 、 。CO2的平衡转化率为 。
②现有两个相同的恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ,在Ⅰ中充入1mol CO2和4molH2,在Ⅱ中充入1mol CH4和2molH2O(g),300℃开始反应,达到平衡时,下列说法正确的是( )(填字母)。
| A.容器Ⅰ、Ⅱ中正反应速率相同 |
| B.容器Ⅰ、Ⅱ中反应的平衡常数相同 |
| C.容器Ⅰ中CO2的物质的量比容器Ⅱ中的多 |
| D.容器Ⅰ中CO2的转化率与容器Ⅱ中CH4的转化率之和小于1 |
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2零排放,其基本原理如下图所示: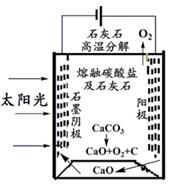
①上述生产过程的能量转化方式是 、 。
②上述电解反应在温度小于900℃时进行,碳酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极电极反应式为 ,阴极电极反应式为 。
某气体的摩尔质量为Mg/mol,分子数目为N,质量为mg,阿伏伽德罗常数为NA,试说明下列各式所表示的意义。
(1)N/NA:(2)M/NA:
(3)m/N:
V L Fe2(SO4)3溶液中,含有Fe3+ m g,则溶液中SO42-的物质的量浓度为__________________
一定的温度和压强下,1体积X2(g)跟3体积Y2(g)化合生成2体积化合物,则该化合物的化学式是_______________
有A、B、C三瓶失去标签的无色溶液:K2CO3、BaCl2、NaOH。将它们分别与稀H2SO4作用,A产生白色沉淀,B产生无色气体,C中无明显现象。
则A是________,B是________ , C是________。
写出反应的化学方程式:
_______________________________________________________
实验室用98%的浓H2SO4(ρ="1.84" g·cm-3)配制1.5 mol·L-1稀H2SO4 溶液100 mL。
溶液100 mL。
(1)计算所需浓H2SO4体积为_________。
(2)量取所需浓H2SO4,应选用________________________。
(3)稀释浓H2SO4的方法(简要操作)_____________________________________________
(4)容量瓶使用前,检验其是否漏水的方法是_________________________________ ______
______
以下操作会引起最后所配溶液的浓度发生什么变化,请填写(偏高、偏低、无影响)
(5)稀释后的浓H2SO4若立即转移至容量瓶中,所配溶液的浓度将_________
( 6)容量瓶用蒸馏洗涤后残留有少量的水________________
6)容量瓶用蒸馏洗涤后残留有少量的水________________
(7)所用过的烧杯、玻璃棒未洗涤________________
(8)定容时俯视刻度线________________