下列应用或事实与胶体的性质没有关系的是
| A.在河流入海口处易形成三角州 |
| B.用石膏或盐卤点制豆腐 |
| C.尿毒症患者做“血液透析” |
| D.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀 |
下列装置或操作能达到实验目的是 ( )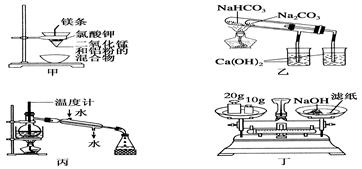
| A.用甲图装置可制得金属锰 | B.用乙图装置验证NaHCO3和Na2CO3的热稳定性 |
| C.用丙图装置分离制取蒸馏水 | D.用丁图装置称量氢氧化钠固体 |
下列物品或设备:①水泥路桥、②门窗玻璃、③水晶镜片、④石英钟表、⑤玛瑙手镯、⑥硅太阳能电池、⑦光导纤维、⑧计算机芯片所用材料为SiO2或要用到SiO2的是 ( )
| A.①②③④⑤⑦ | B.全部 | C.⑥⑧ | D.①②⑦⑧ |
下列叙述正确的是 ( )
A.稀硝酸、稀硫酸均能将木炭氧化成二氧化碳
B.Na2O2与水反应,红热的Fe与水蒸气反应均能生成碱
C.Li、C、P分别在足量氧气中燃烧均生成一种相应氧化物
D.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
小明同学用洁净的铂丝蘸取某无色溶液,在无色火焰上灼烧,火焰呈黄色,通过该实验现象,下列四位同学对该溶液中存在的金属离子的判断正确的是 ( )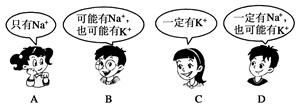
某溶液与Al反应能放出H2,下列离子在该溶液中一定能大量共存的是 ( )
| A.NH4+、Fe2+、NO3-、SO42- | B.Na+、K+、Cl-、SO42- |
| C.Mg2+、H+、Cl-、NO3- | D.K+、Ca2+、HCO3-、Cl- |