用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下列判断正确的是
| A.SO2、CS2、HI都是直线型分子 |
| B.BF3键角为120°,SnBr2键角大于120° |
| C.COCl2、BF3、SO3都是平面三角型分子 |
| D.PCl3、NH3、PCl5都是三角锥型分子 |
元素周期表的第7周期称为不完全周期,若将来发现的元素把第7周期全排满,则下列推论错误的可能性最大的是( )
| A.该周期的元素都是放射性元素 |
| B.该周期的元素,原子序数最大为118 |
| C.该周期的ⅦA族元素是金属元素 |
| D.该周期的ⅢA族的元素的氢氧化物具有两性 |
下列分子中所有原子都满足最外层8电子结构的是()
A PCl5 B HClO C PCl3 D BF3
下列说法正确的是( )
| A.分子晶体中分子间作用力越大,则该物质越稳定 |
| B.乙醇和二甲醚互为同分异构体 |
| C.电子层结构相同的单核离子,阳离子半径一定比阴离子半径大 |
| D.任何原子的原子核都是由质子和中子构成的 |
下列化合物中,含有共价键的离子化合物是()
| A.CCl4 | B.H2SO4 | C.Na2O2 | D.CaCl2 |
下列各项中表达正确的是()
A.F-的结构示意图: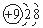 |
B.CO2分子的比例模型示意图: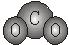 |
C.NaCl的电子式: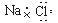 |
D.N2的结构式:∶N≡N∶ |