分析下图所示的四个原电池装置,其中结论正确的是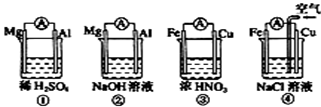
| A.①②中Mg作为负极,③④中Fe作为负极 |
| B.②中Mg作为正极,电极反应式为6H2O + 6e- ═ 6OH- + 3H2↑ |
| C.③中Fe作为负极,电极反应为Fe-2e - ═Fe2+ |
| D.④中Cu作为正极,电极反应式为2H+ + 2e - ═H2↑ |
在许多化合物中S可以取代O,取代后的物质仍跟原化合物具有相似的性质,下面是两种有机磷农药的结构简式: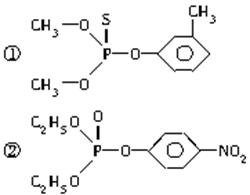
这两种农药在使用过程中不能与下列物质中的哪一种混合使用( )
| A.KCl | B.Ca(OH)2 |
| C.CO(NH2)2 | D.Na2SO4 |
1995年3月20日,在日本东京地铁中发生了震惊世界的“沙林毒气袭击事件”,造成11人死亡,5500多人中毒。恐怖分子使用的“沙林”是剧毒的神经毒剂,它的化学名称为甲氟磷酸异丙酯。已知甲氟磷酸的结构是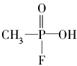 ,则“沙林”的结构简式为( )
,则“沙林”的结构简式为( )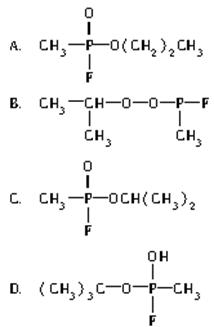
农业生产中用的波尔多液杀菌剂由硫酸铜和石灰乳按一定比例配制而成,它能防治植物病害的原因是( )
| A.硫酸铜使菌体蛋白质盐析 |
| B.石灰乳使菌体蛋白质水解 |
| C.菌体蛋白质能溶解于波尔多液中 |
| D.铜离子和石灰乳使菌体蛋白质变性 |
化合物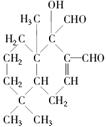 是一种取代有机氯农药DDT的新型杀虫剂,它含有几种官能团( )
是一种取代有机氯农药DDT的新型杀虫剂,它含有几种官能团( )
| A.5种 | B.4种 |
| C.3种 | D.2种 |
水可以造福人类,但水被污染后却给人类造成了灾难,为了防止水污染,下面①~⑤的措施中可以采用的是( )
①禁止使用农药和化肥
②不任意排放工业废水
③抑制水中植物的生长
④生活污水经过净化处理再排放
⑤减少空气中硫的氧化物和氮的氧化物的含量
| A.②③④ | B.②④⑤ |
| C.①④⑤ | D.①②④ |