下列反应的离子方程式不正确的是
| A.碳酸氢钙溶液加入过量的氢氧化钙溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| B.等物质的量的NH4HCO3与NaOH在溶液中反应:NH4++OH-=NH3·H2O |
| C.在含有Mn2+的溶液中加入HNO3酸化,再加入PbO2,反应体系显紫红色:5PbO2 + 2Mn2+ + 4H+ = 5Pb2+ + 2MnO4— + 2H2O |
| D.等体积同浓度NaHSO4、Ba(OH)2两溶液混合:H++SO42—+Ba2++OH—=BaSO4↓+H2O |
某FeSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同,且SO42-的物质的量浓度为6mol•L-1,则此溶液最多溶解铁粉的质量为
| A.11.2g | B.14.0g | C.22.4g | D.33.6g |
在FeCl3和CuCl2混合液中,加入一定量的铁粉,充分反应后,溶液中的金属离子不可能是
| A.仅有Fe2+ | B.有Cu2+ 、Fe2+和Fe3+ |
| C.仅有Cu2+和Fe2+ | D.仅有Fe3+和Fe2+ |
某实验小组对一含有Al3+的未知溶液进行分析,经定量分析后,绘出沉淀的物质的量与滴入氢氧化钠体积的关系图: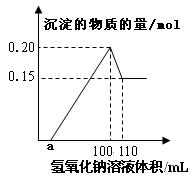
则下列说法中错误的是
| A.该未知溶液中至少含有3种阳离子 |
| B.滴加的NaOH溶液的物质的量浓度为5mol/L |
| C.若另一种离子为二价阳离子,则a="10" |
| D.若将最终沉淀过滤、洗涤、灼烧,其质量一定为6g |
amolNa2O2和bmolNaHCO3混合置于密闭容器中,加热至300℃使其充分反应。密闭容器内固体为Na2CO3和NaOH混合物时,a和b的比值可能是
| A.0.8 | B.1.1 | C.1.8 | D.2.2 |
下列仪器的主要成分不属于硅酸盐材料的是
①冷凝管②明成化斗彩鸡缸杯③石英玻璃 ④计算机芯片⑤光导纤维
| A.③④⑤ | B.②④⑤ | C.①③⑤ | D.②③④ |