化学反应的实质就是旧键的断裂和新键的形成。欲探讨发生化学反应时分子中化学键在何处断裂的问题,近代科技常用同位素示踪原子法。如有下列反应: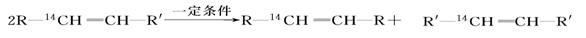
可以推知,物质 发生此反应时断裂的化学键应是
发生此反应时断裂的化学键应是
| A.①③ | B.①④ | C.② | D.②③ |
用石墨作电极电解1 L 1 mol·L-1 CuSO4溶液,当c(Cu2+)="0.5" mol·L-1时,停止电解,向剩余溶液中加入下列何种物质可使电解质溶液恢复至原来状况()
| A.CuSO4 | B.CuO | C.Cu(OH)2 | D.CuSO4·5H2O |
X、Y、Z、M代表四种金属元素。金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为()
| A.X>Z>Y>M | B.X>Y>Z>M | C.M>Z>X>Y | D.X>Z>M>Y |
某原电池总反应离子方程式为2Fe3++Fe====3Fe2+,能实现该反应的原电池是()
| A.正极为Cu,负极为Fe,电解质溶液为FeCl3溶液 |
| B.正极为Cu,负极为Fe,电解质溶液为Fe(NO3)2溶液 |
| C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液 |
| D.正极为Ag,负极为Fe,电解质溶液为CuSO4溶液 |
如下图所示的装置,在铁圈和银圈的焊接处,用一根棉线将其悬吊在盛水的烧杯中,使之平衡。小心地向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是()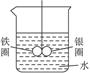
| A.铁圈和银圈左右摇摆不定 | B.保持平衡状况 |
| C.铁圈向下倾斜 | D.银圈向下倾斜 |
下列关于电解法精炼粗铜的叙述中不正确的是()
| A.粗铜板作阳极 |
| B.电解时,阳极发生氧化反应,而阴极发生的反应为:Cu2++2e-====Cu |
| C.粗铜中所含Ni、Fe、Zn等金属杂质,电解后以单质形式沉积槽底,形成阳极泥 |
| D.电解铜的纯度可达 99.95%—99.98% |