下列化学用语或模型正确的是
| A.乙烯的结构简式:CH2CH2 |
B.甲烷分子的比例模型: |
C.羟基的电子式: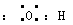 |
| D.葡萄糖的最简式:C6H12O6 |
1 mol某气态烃完全燃烧,生成3 mol二氧化碳和2 mol水,则此烃的分子式是( )
| A.C3H6 | B.C6H6 | C.C3H4 | D.C3H8 |
下列物质之间的相互关系不正确的是( )
A.CH3—CH2—NO2和H2N—CH2—COOH互为同分异构体
B.H、D、T互为同位素
C.O2和O3互为同素异形体 D.-OH、-CHO、-H、-COOH都是官能团
我国稀土资源丰富。下列有关稀土元素 与
与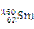 的说法正确的是
的说法正确的是 ()
()
A.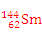 与 与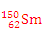 互为同位素 互为同位素 |
B. 与 与 的质量数相同 的质量数相同 |
C. 与 与 是同一种核素 是同一种核素 |
D. 与 与 的核外电子数和中子数均为62 的核外电子数和中子数均为62 |
含有a mol FeBr2的溶液中,通入x mol Cl2,下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是()
| A.x=0.4a,2Fe2++Cl2===2Fe3++2Cl- |
| B.x=0.6a,2Br-+Cl2===Br2+2Cl- |
| C.x=a,2Fe2++2Br-+2Cl2===Br2+2Fe3++4Cl- |
| D.x=1.5a,2Fe2++4Br-+3Cl2===2Br2+2Fe3++6Cl- |
有BaCl2和NaCl的混合溶液aL,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl 离子完全沉淀。反应中消耗xmol H2SO4、ymol AgNO3。据此得知原混合溶液中的c(Na+)/ mol·L-1为()
离子完全沉淀。反应中消耗xmol H2SO4、ymol AgNO3。据此得知原混合溶液中的c(Na+)/ mol·L-1为()
| A.(y-2x)/a | B.(y-x)/a | C.(2y-2x)/a | D.(2y-4x)/a |