已知2Zn(s)+O2(g)= 2ZnO(s);ΔH=-700 kJ/mol,则1 g Zn在氧气中燃烧放出的热量约为
| A.5.4 kJ | B.350 kJ | C.3.5 kJ | D.8.5 kJ |
下列各组性质比较中,正确的是()
①酸性:HClO4>HBrO4>HIO4②碱性:Ba(OH)2>Mg(OH)2>Be(OH)2
③氧化性:F>C>O④还原性:Cl<S<Si
⑤气态氢化物稳定性:HF>HCl>H2S
| A.①②③ | B.②③④ | C.①②④⑤ | D.①②③④⑤ |
阴离子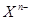 含中子N个,X的质量数为A,a g X的氢化物中含质子的物质的量是( )
含中子N个,X的质量数为A,a g X的氢化物中含质子的物质的量是( )
A.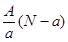 mol mol |
B.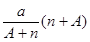 mol mol |
C.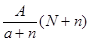 mol mol |
D.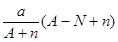 mol mol |
下列各组物质中互为同位素的是()
A.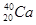 和 和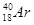 |
B.D和T |
C.H2O和H2O2 | D.O3和O2 |
用质量均为100g的铜作电极,电解硝酸银溶液(足量),电解一段时间后,两电极的质量差为28g,此时两电极的质量分别为( )
| A.阳极100g,阴极128g | B.阳极93.6g,阴极121.6g |
| C.阳极91.0g,阴极119.0g | D.阳极86.0g,阴极114.0g |
浅绿色的Fe(NO3)2溶液中存在着如下的平衡:Fe2++2H2O Fe(OH)2+2H+若在此溶液中加入稀硫酸,则溶液的颜色变化为( )
Fe(OH)2+2H+若在此溶液中加入稀硫酸,则溶液的颜色变化为( )
| A.绿色变深 | B.浅绿色变得更浅 | C.变黄 | D.无明显变化 |