氮氧化物与悬浮在大气中海盐粒子的相互反应:
4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+ Cl2(g),ΔH
2NaNO3(s)+2NO(g)+ Cl2(g),ΔH
在恒温条件下,向2 L恒容密闭容器中加入0.4mol NO2和0.2 mol NaCl,10 min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为α。下列叙述中正确的是
| A.10min内NO浓度变化表示的速率v(NO)=0.01 mol·L-1·min-1 |
| B.若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α |
| C.若升高温度,平衡逆向移动,则该反应的ΔH>0 |
| D.若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行 |
实验测得 BeCl2为共价化合物,两个Be—Cl键间的夹角为180°则BeCl2属于
| A.由极性键构成的极性分子 | B.由极性键构成的非极性分子 |
| C.由非极性键构成的极性分子 | D.由非极性键构成的非极性分子 |
在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是( )
| A.sp,范德华力 | B.sp2,范德华力 |
| C.sp2,氢键 | D.sp3,氢键 |
最近科学家发现一种由钛原子和碳原子构成的气态团簇分子,如图所示,顶角和面心的原子是钛原子,棱的中心和体心的原子是碳原子,则它的化学式是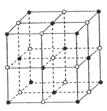
| A.TiC | B.Ti6C7 |
| C.Ti14C13 | D.Ti13C14 |
下列原子或离子原子核外电子排布不属于基态排布的是( )
| A.N: 1s22s22p3 | B.S2-: 1s22s22p63s23p6 |
| C.Na: 1s22s22p53s2 | D.Si: 1s22s22p63s23p2 |
下列事实与氢键有关的是
| A.水加热到很高的温度都难以分解 |
| B.NH3分子极易溶于水 |
| C.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 |
| D.HF、HCl、HBr、HI的热稳定性依次减弱 |