工业上利用废铁屑(含少量氧化铝、氧化铁等)生产硫酸亚铁溶液,进而可制备绿矾(FeSO4·7H2O)、硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐)等重要试剂。生产硫酸亚铁溶液的工艺流程如下:
回答下列问题:
(1)加入少量NaHCO3,调节溶液pH的目的是__________________________。
(2)硫酸亚铁溶液在空气中久置容易变质,用离子方程式表示其变质的原因:_____。
(3)若向所得FeSO4溶液中加入少量3 moL• L-1 H2SO4溶液,再加入饱和(NH4)2SO4溶液,经过蒸发浓缩、冷却结晶、过滤等一系列操作后得到硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐)。硫酸亚铁铵较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液。现取0.352g Cu2S和CuS的混合物在酸性溶液中用40.00 mL0.150 mol•L-1 KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
反应后煮沸溶液,剩余的KMnO4恰好与50.00mL 0.200 mol•L-1 (NH4)2Fe(SO4)2溶液完全反应。
①配平离子方程式:MnO4-+Fe2++H+——Mn2++Fe3++H2O
②Cu2S和CuS的混合物在酸性溶液中用0.150 mol•L-1 KMnO4溶液处理后,溶液需煮沸的原因是:_______________________________________________。
③实验室配制500mL 3 moL• L-1 H2SO4溶液,需要质量分数为98%,密度为1.84g• mL-1硫酸的体积为__________ mL。(保留1位小数)
④试计算混合物中CuS的质量分数(写出计算过程)。
(15分)我国是氧化铝生产大国,工业上每生产1 t氧化铝将排出1~2 t赤泥,赤泥大量堆积会对环境造成严重污染。赤泥中主要成分及含量:CaO约占46%、SiO2约占22%、Al2O3约占7%、Fe2O3约占11%、TiO2约占5%及少量其他物质。
⑴一种利用废弃赤泥的方法是将赤泥配成一定的液固比,作为一种吸收剂,吸收热电厂排放的含SO2的烟气,写出吸收SO2时可能发生的化学反应方程式______________________。
⑵为综合利用赤泥中的各种成分,某科研小组设计了如下工艺流程:
已知:TiO2不溶于稀盐酸、稀硫酸,能溶于浓硫酸生成TiOSO4(硫酸氧钛,易水解)。
①氧化物D的化学式是_____________,原料A最好是下列物质中的____________。
| A.氨水 | B.氢氧化钠 | C.生石灰 | D.双氧水 |
②写出上述工艺中投入氢氧化钠时反应的离子方程式:
______________________________________________________。
③写出上述工艺中稀释时发生水解反应的化学方程式:
______________________________________________________。
气体X对氢气的相对密度为22。X可由下列步骤合成(cat表示催化剂):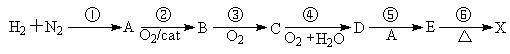
试根据题意回答下列问题:
(1)X的化学式为 ;X与CO2互为等电子体,所以可推测其分子结构呈 (型)。
(2)液态时的A能与金属钠反应生成F,熔融态的F能与X反应,其中生成一种固体G。G在受撞击时,生成两种单质,其中一种单质能与Li在常温下反应。试写出F+X→G的化学反应方程式 。
(3)D在较稀浓度(2mol/L)时能与Mg反应生成X。试写出化学反应方程式 。
(4)实验室制备少量的X,可将B通入K2SO3溶液中制得。请写出该反应的化学方程式 。
(7分)(1)往铜和稀硫酸的混合物中加入双氧水溶液,可以观察到的实验现象是:溶液变蓝,并产生无色气体,请写出涉及这一现象的所有化学反应方程式:
, 。
(2)两个氧化还原反应的离子方程式如下:
① R3++Cl2+6OH-=RO3-+2Cl-+3H2O
② 5RO3-+2Mn2++14H+=5R3++2MnO4-+7H2O
由此 (填“能”或“不能”)得出Cl2的氧化性比MnO4-强的结论,理由是 。
今有两种溶液A、B,共含有较多量的H+、K+、Na+、Mg2+、Fe3+和Cl-、OH-、NO3-、S2-、SO32-十种离子。在两种溶液里所含上述离子各不相同,其中A溶液里含有三种阳离子和两种阴离子,它们是______,其余离子在B溶液里,它们是______。
(8分)在密闭容器中,由一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内的分压与反应温度的关系如右图所示(已知气体的分压之比等于物质的量之比。)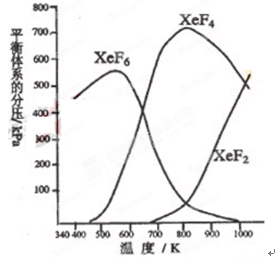
(1) 420K时,发生反应的化学方程式为:;若反应中消耗1 mol Xe,则转移电子mol。
(2) 600K—800K时,会发生反应:
XeF6(g) XeF4(g)+F2(g),
XeF4(g)+F2(g),
其反应热DH0(填“>”、“=”或“<”)。理由是。
(3) 900K时,容器中存在的组分有。