(12分)电化学原理常应用于工农业生产、对工业废水和生活污水进行处理。
(1)对工业废水进行处理是防止水体污染、改善水质的主要措施之一,含氰废水中的CN-有剧毒。
①CN-中碳元素显+2价,则非金属性N C(填<,=或>)
②在微生物的作用下,CN-能够被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为 。
(2)某研究性学习小组模拟工业生产,将下列装置如图连接,C、D、E、X、Y 都是石墨,F是铁,丙是模拟精炼铜。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题: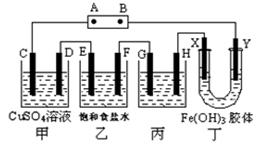
①电源 B 极的名称是________
②甲装置中电解反应的总化学方程式是:___________ _。
③通电一段时间后,丙中原电解质的物质的量浓度将__________(填“变大”、“变小”或“不变”)。
④装置丁中的现象是_________________________________ _______。
(3)对生活污水进行处理是防止水体污染、改善水质的主要措施。电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA”表示乳酸分子,A- 表示乳酸根离子)。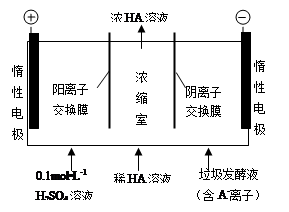
① 阳极的电极反应式为 。
② 电解过程中,采取一定的措施可控制阳极室的pH约为6-8,此时进入浓缩室的OH-可忽略不计。400mL 10 g•L-1乳酸溶液通电一段时间后,浓度上升为145 g•L-1(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为 L。(乳酸的摩尔质量为90 g• mol-1)
(8分)已知有以下的物质相互转化关系,A是常见的金属单质,能被磁铁吸引。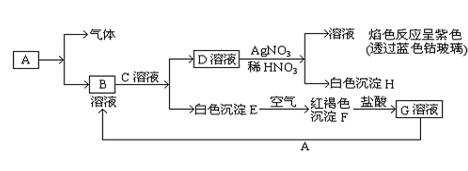
(1)试回答: 写出B的化学式H的化学式。
⑵ 写出由E转变成F的化学方程式。
⑶向G溶液加入A的有关离子反应方程式____。
阅读下面两条科普信息,回答问题:
(1)一个体重50Kg的健康人含铁2g,这2g铁在人体中不是以单质金属的形式存在,而是以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(2)在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿;该反应的另一种反应物是CO2,反应后CO2转变成有机物(用甲醛:CH2O表示)。
问题:
这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实、方法和途径。这说明亚铁离子具有性,铁离子具有性
(1)中的维生素C是剂,(2)中的CO2剂。
(4分)配平氧化还原反应方程式。
(1) NH3+ NO2— N2+ H2O
(2) 氧化产物与还原产物的质量比为 。
10分)某化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水成分搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是__________________________ ___ ______。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是_________________________ ______。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。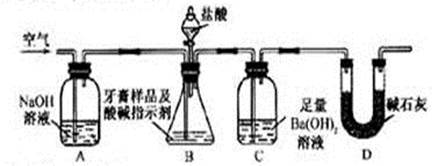
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:_________________________________。
(4)C中反应生成BaCO3的化学方程式是_______________________ _________。
(5)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为_________。
1g甲烷完全燃烧生成CO2气体和液态水时放出QkJ热量,则甲烷燃烧的热化学方程式为。