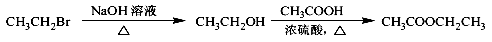(14分)已知A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1 mol丁分子中不同原子的数目比为1:2,且含有18 mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用。各物质间的转化关系如下图所示(某些条件巳略去)。
请回答:
(1)写出B单质的电子式 。写出丙的结构式 。
(2)戊与强碱反应的离子方程式:____________________________。
(3)丁中所包含的化学键类型有_____________ (填字母序号)。
A.离子键 B.极性共价键 C.非极性共价键
(4)利用单质B与H2为原料、含H+的固体物质作电解质,在常压下用H2和用He气稀释的单质B分别通入电解池的两极,在570℃时进行反应,反应物转化率高达78%,则生成产物的电极上的电极反应式为 ,另一个电极上的电极反应类型是 。
(5)反应②中,0.5mol NaClO参加反应时,转移1 mol电子,其化学方程式为:_______________。
(6)—定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。巳知,该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为: _________________。
(10分)某合成树脂E的单体A(C3H4O2),存在如下转化关系: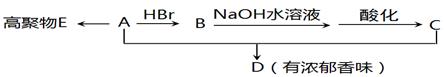
已知:①A能使溴的CCl4溶液褪色,又能与碳酸钠溶液反应放出CO2
②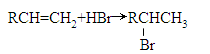 ③
③ (X指卤素原子)
(X指卤素原子)
回答下列问题:
(1)A中官能团的名称是 。
(2)A+C→D的化学方程式 。
(3)E的结构简式 。
(4)下列化合物中属于B的同分异构体的是 。
A.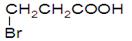 B.
B.
C.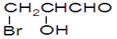 D.
D.
(5)对于化合物D,下列说法正确的是 。
A.能发生水解反应 B.能与乙酸发生酯化反应
C.不能使酸性KMnO4溶液褪色 D.不能与金属钠反应放出气体
(9分)甲、乙、丙均为化合物,其中甲为淡黄色的固体,乙常温下为无色无味液体,丙为常见的无色无味气体。它们有如下图的转化关系,已知D为黄绿色气体,按要求回答下列问题: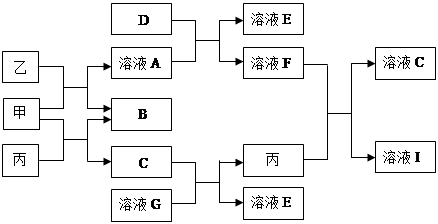
(1)甲物质为_____________(填化学式)。
(2)1mol乙和足量甲反应可生成______________mol B物质;1mol丙和足量甲反应可生成____________mol B物质。
(3)D能使湿润的有色布条褪色,其褪色原因是______________________。
(4)丙与溶液F反应的化学方程式为_____________________。
【化学——选修5:有机化学基础】有机物A为烃类化合物,质谱图表明其相对分子质量为70,其相关反应如下图所示,其中B、D、E的结构中均含有2个—CH3,它们的核磁共振氢谱中均出现4个峰。
请回答:
(1)B中所含官能团的名称为 ; D的分子式为 ;
(2)Ⅲ的反应类型为 (填字母序号);
a.还原反应 b.加成反应c.氧化反应 d.消去反应
(3)写出下列反应的化学方程式:
Ⅰ: ;Ⅱ: ;
(4)C和E可在一定条件下反应生成F,F为有香味的有机化合物,该反应的化学方程式为 ;
(5)A的同分异构体中有一对互为顺反异构,且结构中有2个—CH3,它们的结构简式为 和 ;
(6)E的另一种同分异构体能发生银镜反应,能与足量金属钠生成氢气,不能发生消去反应,其结构简式为 。
常见的五种盐X、Y、Z、M、N,它们的阴离子可能是SO42-、Cl-、NO3-、CO32-,阳离子可能是Ag+、NH4+、Na+、Al3+、Cu2+、Ba2+、Fe3+,已知:
①M的焰色反应呈黄色。
②五种盐均溶于水,水溶液均为无色。
③X的溶液呈中性,Y、Z、N的溶液呈酸性,M的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有X、Z的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,N和Z的溶液中生成沉淀,继续加氨水,Z中沉淀消失。
⑥把X的溶液分别加入到Y、Z、N的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定不含有的阳离子是_________;所含阴离子相同的两种盐的化学式是_____________。
(2)M的化学式为_______________,M溶液显碱性的原因是________________(用离子方程式表示)。
(3)X和Z的溶液反应的离子方程式是______________;N和氨水反应的离子方程式是__________________。
(4)若要检验Y中所含的阳离子,正确的实验方法是______________________。
一种重要的有机化工原料有机物X,下面是以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。Y是一种功能高分子材料。
已知:(1)X为芳香烃,其相对分子质量为92
(2)烷基苯在高锰酸钾的作用下,侧链被氧化成羧基:
(3) (苯胺,易被氧化)
(苯胺,易被氧化)
请根据本题所给信息与所学知识回答下列问题:
(1)X的分子式为______________。
(2) 中官能团的名称为_________________;
中官能团的名称为_________________;
(3)反应③的反应类型是___________;已知A为一氯代物,则E的结构简式是____________;(4)反应④的化学方程式为__________________;
(5)阿司匹林有多种同分异构体,满足下列条件的同分异构体有________种:
①含有苯环;②既不能发生水解反应,也不能发生银镜反应;③1mol该有机物能与2molNaHCO3完全反应。
(6)请写出以A为原料制备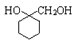 的合成路线流程图 (无机试剂任用)。
的合成路线流程图 (无机试剂任用)。
合成路线流程图示例如下: