(10分)汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NOx等有毒气体,其污染问题也成为当今社会急需解决的问题。
(1)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图: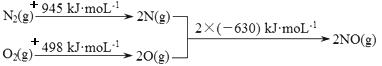
则该反应的热化学方程式为 。
(2)对汽车加装尾气净化装置,可使CO、NOx有毒气体相互反应转化为无毒气体。
2xCO+2NOx ==2xCO2+N2,当转移电子物质的量为0.6x mol时,该反应生成标准状况下N2 L。
(3)一氧化碳是一种用途相当广泛的化工基础原料。可以还原金属氧化物,还可以用来合成很多有机物如甲醇等。在压强为0.1 MPa条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下反应生成甲醇:
O(g)+2H2(g)  CH3OH(g);△H= -bkJ•mol-1
CH3OH(g);△H= -bkJ•mol-1
①该反应的平衡常数表达式为 。
②若容器容积不变,下列措施可增加甲醇产率的是 。
| A.升高温度 | B.将CH3OH(g)从体系中分离 |
| C.缩小体积,增大压强 | D.再充入1 mol CO和3 mol H2 |
③经测定不同温度下该反应的平衡常数如下:
| 温度(℃) |
250 |
300 |
350 |
| K |
2.041 |
0.270 |
0.012 |
若某时刻250℃测得该反应的反应物与生成物的浓度为c(CO)=0.8 mol/L、c(H2)=1.0mol/L、c(CH3OH)=0.8 mol·L-1,则此时v正 v逆(填>、<或=)。
(选做题)鲜榨苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色Fe3+。这个变色的过程中的Fe2+被(填“氧化”或“还原”)。若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生。这说明维生素C具有:。
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
维生素C主要存在于蔬菜、水果中,它能增加人体对疾病的抵抗能力。其结构简式为
请回答:
(1)维生素C的分子式是,其分子中不含氧的官能团的名称是。
(2)维生素C可发生的化学反应有(填序号)。
①加成反应②氧化反应③酯化反应
(3)向维生素C的水溶液中滴加紫色石蕊试液,试液变红,说明维生素C的水溶液显性。
下表是元素周期表的一部分,按要求填空(填元素符号或化学式):
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
① |
② |
||||||
| 3 |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
|
| 4 |
⑩ |
(11) |
(12) |
(1)写出下列元素的元素符号:①②(11)
(2)在这些元素中,最活泼的金属元素是,最活泼的非金属元素是,最不活泼的元素是。
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是,碱性最强的是,呈两性的氢氧化物是。
元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。请依据元素周期表回答问题。
(1)填写下表
| 元素 |
甲 |
乙 |
丙 |
丁 |
| 原子序数 |
6 |
13 |
||
| 元素周期表中的位置 |
第二周期 第VIA族 |
第三周期 第IA族 |
(2)丙的原子结构示意图是,该元素与同周期VIIA族元素组成的化合物类型是。
原电池是把转化成的装置,其反应的实质是。在铜锌原电池(稀硫酸为介质)中:
正极材料是,其电极反应式:;
负极材料是,其电极反应式:;