X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7价。回答下列问题:
(1)元素X原子结构示意图为__________。
(2)元素Y的一种同位素可测定文物年代,这种同位素的符号是________。
(3)元素Z能与氢元素形成+1价阳离子,每个该离子中的电子数是________,元素Z的最高价含氧酸的稀溶液与金属银反应的离子方程式为_______________________________。
(4)元素W的单质与元素X的低价氧化物在水溶液中反应的离子方程式
_____________________________________________________________________;
元素X的气态氢化物与过氧化氢溶液混合后有浅黄色固体生成,请写出发生的化学方程式____________________________。
(5)探寻物质的性质差异性是学习的重要方法之一。X、Y、Z、W四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是________(用酸的分子式表示)。
恒温、恒压下,在一个可变容积的容器中发生如下反应:
A(气)+B(气) C(气)。
C(气)。
I(1)若开始时放入1molA和1molB,到达平衡后,生成amolC,这时A的物质的量为_______________mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为______mol。
(3)若开始时放入xmolA、2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3amol,则x=________mol,y=________mol。平衡时,B的物质的量____________(选填一个编号)
(甲)大于2mol(乙)等于2mol
(丙)小于2mol(丁)可能大于、等于或小于2mol
作出此判断的理由是__________________________。
(4)若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是_________________。
II 若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。
(5)开始时放入1molA和1molB到达平衡后生成bmolC.将b与(1)小题中的a进行比较__________(选填一个编号)
(甲)a<b(乙)a>b(丙)a="b" (丁)不能比较a和b的大小
作出此判断的理由是_______________________________。
A.B.C.D.E是中学化学常见单质,构成它们的元素的原子序数分别为α、b. c.d.е;且3 (a+b) =" 2" (a+c) =" 3" (d-a);X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系(图中反应物和产物中的H2O已略去):
(1)Y的电子式为,构成D单质的元素在周期表中位于周期族。
(2)反应③的离子方程式为E的氧化物与D在一定条件下反应的化学方程式为:。
(3)固体N常温下即挥发,183℃升华,几乎溶于所有的有机溶剂和H2O中,据此判断
N为型晶体。
(4)25℃时,PH=5的W和N的水溶液中由H2O电离出来的H+离子浓度之比为。
(12 分)卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)基态溴原子的电子排布式为。
(2)卤素互化物如BrI、ICl等与卤素单质结构相似、性质相近。Cl2、BrI、ICl沸点由高到低的顺序为。
(3)多卤化物RbICl2加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,A的化学式为。
(4)I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为。
(5)气态氟化氢中存在二聚分子(HF)2,这是由于。
(6)①HClO4、②HIO4、③H5IO6[可写成(HO)5IO]的酸性由强到弱的顺序为 (填序号)。
合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氮气直接合成氨,制得的氨通过催化氧化可生产硝酸。
在一定条件下,若N2和H2以体积比1:3的比例充入一体积不变的密闭容器中反应,达到平衡状态时,测得混合气体中氨的体积分数为20.0%,则:
(1)合成氨反应达到平衡的标志 ▲。
| A.容器内气体压强保持不变 |
| B.容器内各物质的浓度不随时间变化 |
| C.当υ(H2,正)=0.3mol·L-1·min-1,υ(NH3,逆)=0.2mol·L-1·min-1时 |
| D.1个N≡N键断裂的同时,有3个H-H键形成 |
(2)达到平衡时,N2和H2的转化率分别为 ▲。
(3)用氨催化氧化可生产硝酸,取所生产的硝酸溶液100mL,与足量的铜反应,生成的NO2和NO混合气体在标准状况下体积为6.72L,物质的量之比为2:1,求所生产硝酸的物质的量浓度?(请写出该小题的计算过程)
▲。
(4)某厂用NH3生产硝酸,然后再制硝酸铵,其过程如下: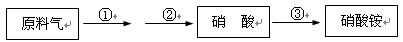
其中反应②为:4NO+3O2+2H2O 4HNO3,原料气为氨气和空气的混合物。
4HNO3,原料气为氨气和空气的混合物。
若实际生产中,反应①、②、③的转化率(或利用率)分别为a、b、c,则生产硝酸的氨气占所用氨气总量的体积分数为 ▲。
(12 分)某芳香烃的分子式为C12H14,其苯环上的一氯代物只有一种,A能发生如下图所示的转化,并最终制得合成纤维J和合成橡胶K。(某些反应条件已略去)
已知:


Ⅰ.请回答下列问题:
(1)A的结构简式 ▲。
(2)上述转化发生的反应中,属于消去反应的是 ▲。
(3)反应⑨的化学方程式是 ▲。
(4)请写出两种符合下列条件的B的同分异构体的结构简式:
①能与FeCl3溶液反应显色;②能与溴的CCl4溶液发生加成反应;③苯环上有三个取代基。
▲、 ▲。
Ⅱ.3-戊醇可作香料。以甲醛和乙炔钠为原料,其他试剂自选,完成其合成路线。 ▲。
▲。