(14分)下图是某实验小组探究FeSO4固体分解的实验装置。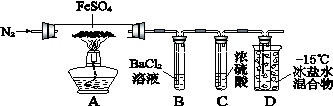
| |
实验过程 |
实验现象 |
| ① |
通入一段时间N2,加热 |
A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
| ② |
用带有火星的木条靠近装置D的导管口 |
木条复燃 |
| ③ |
充分反应,停止加热,冷却后,取A中固体,加盐酸 |
固体溶解,溶液呈黄色 |
| ④ |
将③所得溶液滴入D试管中 |
溶液变为浅绿色 |
已知:SO2熔点–72℃,沸点–10℃;SO3熔点16.8℃,沸点44.8℃。
(1)加热前通入一段时间N2目的是__________________________________。
(2)实验③反应的离子方程式是__________________________________。
(3)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有______气体,依据是_________________________________。
(4)实验④反应的离子方程式是___________________________________________。
(5)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,原因是(用必要的文字和化学方程式解释)__________________________________。
(6)有人认为省略B装置同样可以检验是否有产物SO3,若你认为正确,理由是(若你认为不正确,此问不答。)___________________________________________。
在实验室制各氯气的实验中:制法
(1)反应原理(方程式)为
(2)实验装置如图所示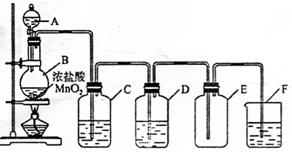
指出下列装置中所盛试剂及其作用:
C.
D.
F.
下面是某化学兴趣小组的同学做同周期元素性质递变规律实验时,设计了一套实验方案。其中实验步骤如下:
| 实验序号 |
实验步骤 |
| ① |
将镁条用砂纸打磨后,放入沸水中,再向溶液中滴加酚酞溶液 |
| ② |
向新制得到的Na2S溶液中滴加新制的氯水 |
| ③ |
将一小块金属钠放入滴有酚酞溶液的冷水中 |
| ④ |
将镁条投入稀盐酸中 |
| ⑤ |
将铝条投入稀盐酸中 |
⑴实验目的
⑵写出实验①和②中的实验现象和化学方程式
实验①:现象化学方程式
实验②:现象化学方程式
⑶实验结论
实验室用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的烧碱溶液进行反应,通过测定反应过程中的放热来计算中和热。试回答下列问题:
(1)在本实验中除了用到大烧杯、小烧杯、温度计、量筒等仪器外,还须的一种玻璃仪器名为。
(2)两只烧杯间要填满碎纸条,其目的是;
(3)大烧杯上必须盖上硬纸板,否则,求得的中和热数值将(填“偏大”、“偏小”、“无影响”)。
(4)实验时所用盐酸及NaOH溶液的体积均为50mL,各溶液密度为1g/cm3,生成溶液的比热容C=4.18J/(g·℃),实验起始温度为t1℃,终止温度为t2℃。试推断中和热的计算式:△H=。
(5)实验中改用52mL 0.50mol/L的盐酸与50mL 0.55mol/L的烧碱溶液反应,与上述实验相比,所放出的热量(填“相等”“不相等”),所求中和热(填“相等”“不相等”)简述理由
(6)用相同浓度和体积的氨水代替烧碱溶液进行上述实验,测得的中和热的数值会;若改用50mL 0.50mol/L烧碱溶液进行上述实验,测得的中和热的数值会。(填“偏大”、“偏小”、“无影响”)
(1)欲量取20.00mL Na2CO3溶液,应选用的仪器是_________________。
(2)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、____________________。
(3)在测定硫酸铜晶体中结晶水含量的实验中,称量晶体和晶体受热失去结晶水都是在______中(填仪器名称)进行。
鸡蛋壳中含有大量钙、少量镁和钾等元素。实验室可用图示流程测定鸡蛋壳中钙、镁元素含量。依据的反应可以表示为:Ca2++Y2-=CaY、Mg2++Y2-=MgY。回答下列问题。
(1)测定Ca2+、Mg2+总含量时,控制溶液pH=10。若pH过大,测定结果将(填“偏大”、“偏小”或“无影响”)。
(2)如果鸡蛋壳粉质量为m g,溶液中Y2+浓度为c mol/L,则鸡蛋壳样品中镁元素质量分数是。
(3)有同学提出可采用如下装置,通过测定鸡蛋壳与盐酸反应产生的二氧化碳的量就能测定鸡蛋壳中的钙的总含量。
①采用该方法进行实验,各装置从左到右的连接顺序依次1→2→____________(填各装置对应接口的数字序号)。
②若排除实验仪器和操作的影响因素,此实验方法测得的结果是否准确?答:________(填“准确”、“不准确”或“无法判断”)。原因是。