下列化学用语中,不正确的是
A.氯原子结构示意图: |
B.HCl的电子式: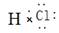 |
| C.乙烯的结构简式:CH2=CH2 |
D.乙炔的比例模型: |
化学与生产、生活密切相关。下列叙述正确的是
| A.淀粉、油脂和蛋白质都是天然高分子化合物 |
| B.葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 |
C. 可用于文物年代的鉴定, 可用于文物年代的鉴定, 与 与 互为同素异形体 互为同素异形体 |
| D.从海水中可以得到NaCl,电解饱和NaCl溶液可以得到金属Na |
某温度下,H2(g)+CO2(g) H2O(g)+CO(g)的平衡常数K=9/4,该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示,下列判断不正确的是
H2O(g)+CO(g)的平衡常数K=9/4,该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示,下列判断不正确的是
| 起始浓度 |
甲 |
乙 |
丙 |
| c(H2)/mol·L-1 |
0.010 |
0.020 |
0.020 |
| c(CO2)/mol·L-1 |
0.010 |
0.010 |
0.020 |
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol·L-1
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
绿原酸的结构简式如图,下列有关绿原酸的说法不正确的是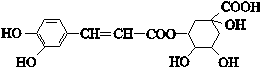
| A.分子式为C16H18O9 |
| B.能与Na2CO3反应 |
| C.能发生取代反应和消去反应 |
| D.0.1 mol绿原酸最多与0.8 mol NaOH反应 |
关于下列各图的叙述,正确的是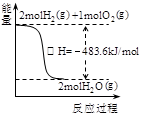
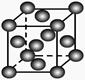
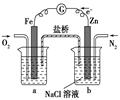
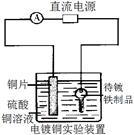
甲乙丙丁
| A.甲表示H2与O2发生反应过程中的能量变化,则H2的烧热为483.6kJ·mol-1 |
| B.乙表示Cu形成金属晶体时的堆积方式 |
| C.丙装置中烧杯a中的溶液pH降低 |
| D.丁装置中待镀铁制品应与电源正极相连 |
若NA为阿伏加德罗常数的值,下列说法正确的是
| A.NA个Fe(OH)3胶体粒子的质量为107g |
| B.8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA |
| C.标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA |
| D.2.3gNa与氧气完全反应,反应中转移的电子数介于0.1NA到0. 2NA之间 |