已知短周期主族元素X、Y、Z在元素周期表中的位置如下图,
下列说法正确的是
| A.原子半径Y>X>Z |
| B.X元素一定是非金属元素 |
| C.当X、Y、Z为非金属时,气态氢化物的稳定性:Y>X>Z |
| D.Z的原子序数可能是X的原子序数的2倍 |
根据下列有关图象,说法正确的是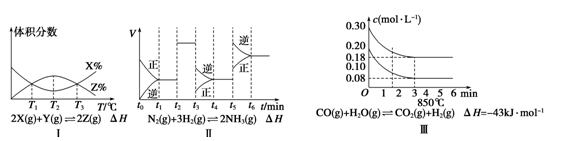
| A.由图Ⅰ知 ,反应在T1、T3处达到平衡,且该反应的ΔH<0 |
| B.由图Ⅱ知,反应在t6时刻,NH3体积分数最大 |
| C.由图Ⅱ知,t3时采取降低反应体系温度的措施 |
| D.图Ⅲ表示在10 L容器、850℃时的反应,由图知,到4 min时,反应放出51.6 kJ的热量 |
一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g) 3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a %。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a %的是
3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a %。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a %的是
A.2 mol C
B.1 mol A、1 mol B和1 mol He(不参加反应)
C.1 mol B和1 mol C
D.2 mol A、3 mol B和3 mol C
某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g) 2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则
2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则
A.平衡不移动
B.再达平衡时,n(A)∶n(B)∶n(C)仍为2∶2∶1
C.再达平衡时,C的体积分数增大
D.再达平衡时,正反应速率增大,逆反应速率减小
反应N2O4(g) 2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。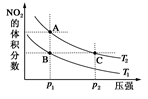
下列说法正确的是
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
如图表示反应2 SO2(g)+O2(g)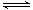 2 SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是
2 SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是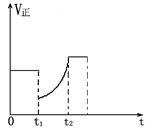
| A.t1时减小了SO2的浓度,增加了SO3的浓度,平衡向逆反应方向移动 |
| B.t1时降低了温度,平衡向正反应方向移动 |
| C.t1时减小了压强,平衡向逆反应方向移动 |
| D.t1时增加了SO2和O2的浓度,平衡向正反应方向移动 |