(14)硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用。
(1)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池的负极的电极反应式 。
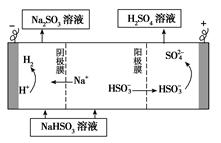
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如下图所示。电解时阳极区会产生气体,产生气体的原因是 。
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:
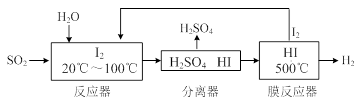
①用离子方程式表示反应器中发生的反应 。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是 。
(3)氢化亚铜是一种红色固体,可由硫酸铜为原理制备
4CuSO4 + 3H3PO2 + 6H2O =" 4CuH↓" + 4H2SO4 + 3H3PO4。
①该反应氧化剂是 (写化学式)。
②该反应每生成1molCuH,转移的电子物质的量为 。
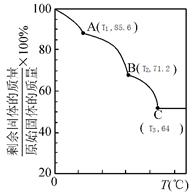
(4)硫酸铜晶体常用来制取波尔多液,加热时可以制备无水硫酸铜,下图是硫酸铜晶体受热分解图示。
请写出A→B的方程式 。
(CN)2、(OCN)2、(SCN)2等通称为拟卤素,它们的性质与卤素相似,氧化性强弱顺序是:(OCN)2>Cl2>(CN)2>(SCN)2>I2,写出下列反应的方程式
(1)(OCN)2 + KI
(2)AgCN
(3)(SCN)2 + H2O
原电池的正极__________(填“得到”或“失去”)电子,发生__________(填“氧化”或“还原”)反应;负极__________(填“得到”或“失去”)电子,发生__________(填“氧化”或“还原”)反应。
中国海水资源丰富,回答下列问题:
(1)海水中主要含有 等离子(写离子符号,至少答出4种)。
(2)海水脱硫是一种有效除去火力发电产生的SO2的方法。其工艺流程如下图所示:
天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是: ;氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是 。
(3)下图是海水综合利用的一个方面。
请回答下列问题:
I.①步主要反应的离子方程式: 。
溴及其化合物的用途有很多,写出其中的一种 。
II.第③步需要加入 ,其前面分离出氢氧化镁的操作称为 ,将镁条在二氧化碳中燃烧的产物为 。
III.粗盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤正确的操作顺序是
一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+ Fe3+。在过程A中,Fe2+作 剂。
Fe3+。在过程A中,Fe2+作 剂。
维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有 性。
(2)某些补铁剂的成分是硫酸亚铁,长期放置会因氧化而变质。检验硫酸亚铁是否变质的试剂是______________(填序号)。
①稀盐酸 ②石蕊溶液 ③KSCN溶液
(3)要除去FeCl3溶液中少量的氯化亚铁,可行的办法是 (填字母)。
a.加入铜粉 b.加入铁粉 c.通入氯气 d.加入NaOH溶液
根据选用的试剂,写出该过程中发生反应的离子方程式 。
(4)电子工业常用30%的FeCl3 溶液腐蚀铜箔,制造印刷线路板,写出FeCl3 与金属铜反应的离子方程式 。
甲、乙、丙、X是中学化学中常见的物质,在一定条件下,它们之间的转化关系如下图所示(部分产物已略去)。请回答下列问题:
(1)若X是 O2,则甲不可能是_______________(填代号)
a.Mg b.N2 c.S d.Al
(2)若甲能使湿润的红色石蕊试纸变蓝,丙为红棕色气体。写出甲转化为乙的化学方程式:________________________。
(3)若乙是一种常见的温室气体,则X的化学式为__________。
(4)若丙为淡黄色粉末,常用作呼吸面具中的供氧剂,则丙与水反应的离子方程式为____________;1mol丙与水发生反应时转移电子的物质的量为____________mol。
(5)若X是一种常见的金属单质,常温下甲的浓溶液可盛放在铝制容器中,丙为浅绿色溶液。
①检验乙是否完全转化为丙的试剂为________________(填试剂名称)。
②保存丙溶液常加入少量X,其目的是__________________。