某溶液中含有HCO3-、Na+、Ba2+、NO3-4种离子,若向其中加入少量Na2O2固体后溶液中离子浓度基本保持不变的是
| A.HCO3- | B.Na+ | C.Ba2+ | D.NO3- |
对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是()
4NO(g)+6H2O(g),下列叙述正确的是()
| A.反应达到平衡时,若两种反应物的转化率相等,则起始投入的n(NH3)∶n(O2)=4∶5 |
| B.反应达到平衡后,对体系一直进行加压,平衡总是逆向移动 |
| C.反应达到平衡时,若向压强固定的密闭容器中充入稀有气体,平衡不移动 |
| D.当v正(NH3)∶v正(NO)=1∶1时,说明该化学反应已经达到平衡 |
25℃时,在等体积的①pH=0的H2SO4溶液②0.05 mol·L-1的Ba(OH)2溶液 ③pH=10的Na2S溶液 ④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是()
| A.1∶10∶1010∶109 |
| B.1∶5∶5×109∶5×108 |
| C.1∶20∶1010∶109 |
| D.1∶10∶104∶109 |
下表是三种难溶金属硫化物的溶度积常数(25 ℃)。
| 化学式 |
FeS |
CuS |
MnS |
| 溶度积 |
6.3×10-18 |
1.3×10-36 |
2.5×10-13 |
下列有关说法中正确的是()
A.25 ℃时,CuS的溶解度大于MnS的溶解度
B.25 ℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-36 mol·L-1
C.因为H2SO4是强酸,所以反应CuSO4+H2S===CuS↓+H2SO4不能发生
D.除去某溶液中的Cu2+,可以选用FeS作沉淀剂
白磷与氧气可发生如下反应:P4+5O2===P4O10。已知断裂下列化学键需要吸收的能量分别为P-P:a kJ· mol-1、P-O:b kJ· mol-1、P=O:c kJ· mol-1、O=O:d kJ· mol-1。根据下图所示的分子结构和有关数据估算该反应的ΔH,其中正确的是()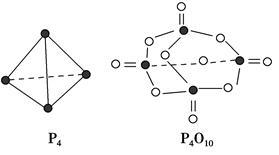
| A.(6a+5d-4c-12b) kJ· mol-1 |
| B.(4c+12b-6a-5d) kJ· mol-1 |
| C.(4c+12b-4a-5d) kJ· mol-1 |
| D.(4a+5d-4c-12b) kJ· mol-1 |
室温下,对于0.10mol·L-1的氨水,下列判断正确的是()
| A.与AlCl3溶液发生反应的离子方程式为Al3++3OH-===Al(OH)3↓ |
| B.加水稀释后,溶液中c(NH4+)·c(OH-)变大 |
| C.用HNO3溶液完全中和后,溶液不显中性 |
| D.其溶液的pH=13 |