(I)在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气;则
(1) 烧杯中放入锌的质量大(填甲或乙);
(2) 烧杯中的酸过量(填甲或乙);
(3)反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+) (填大或小)
(II)物质的量浓度相同的等体积的两份溶液A和B,A为盐酸,B为醋酸,分别和等质量的Zn反应,则下列说法正确的是:
①产生的H2质量一定相同 ②产生H2的质量一定不同
③仅有一份溶液中存在锌,则一定是盐酸 ④等倍数稀释后的反应速率A>B
⑤产生等量H2所需时间A>B ⑥产生等量H2,盐酸和醋酸一定都有剩余
(III)向体积都为1L,pH都等于2的盐酸和醋酸溶液中投入0.3g Zn,则下图中比较符合客观事实的曲线是_________________。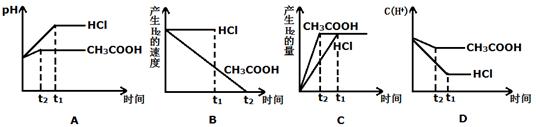
下列A~G均是中学常见化合物,它们之间有如图的转化关系(部分反应物或生成物略去),已知B为一种气体,E、F、G三种化合物中均含有同一种元素M,且价态互不相同。请回答下列问题。
(1)M元素为____________。
(2)B是_________或_________,写出两种鉴别它们的方法________;____________。
(3)若A与G反应也能制B,且反应中n(A):n(G)=1:2,则此时该反应的离子方程式是________________________。
(4)若B与F在一定条件下反应生成一种化合物和一种单质,该反应的化学方程式为________________________。
X、Y、Z、W是原子序数依次增大的短周期元素,互不同族,其中只有两种为金属元素;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。Y和W的单质都能与NaOH溶液反应。请回答下列问题:
(1)X元素的名称是_________,Y、Z、W的原子半径由小到大的顺序是________(用元素符号表示)。
(2)W元素在周期表中的位置是__________,Y元素的原子结构示意图是___________。
(3)Z和W在一定条件下能形成化合物ZW2,分子中各原子均达到了8电子稳定结构,则ZW2的电子式是_______;它在常温下呈液态,形成晶体时,属于________晶体。
(4)X的单质与Y的单质化学性质相似,则X的单质与NaOH溶液反应的离子方程式是_______________(注:生成物中,含有X元素的化合物的化学式中含有2个氧原子)
(5)0.1mol W的单质与50 mL 1.5 mol·L-1的FeBr2溶液反应,被氧化的Fe2+和Br-的物质的量之比是____________。
芳香酯类化合物A、B互为同分异构体,均含C、H、O三种元素。相同状况下A、B蒸汽对氢气的相对密度都是97,分子中C、H原子个数相同,且C、H原子总数是氧原子数的5倍。
已知:各有机物之间存在如下转化关系
其中C能发生银镜反应,F经连续氧化可生成C;C与D是相对分子质量相同的不同类有机物。
(1)A的分子式是。
(2)E中所含官能团的名称是。完全燃烧时,1mol D 与1 mol 下列
的耗氧量相同(填字母代号)。
a. C3H6O3 b. C3H8O c. C2H4 d. C2H6O2
(3)B的结构简式是。
水杨酸与小苏打反应的化学方程式是。
C与F反应的化学方程式是,反应类型是。
(4)同时符合下列要求的同分异构体有种。
①与A互为同分异构体②可以水解③苯环上有两个取代基,且苯环上的一氯
代物只有1种。
(5)1 mol 上述(4)中的一种有机物X,能与4 mol NaOH发生反应,写出此反应的化学方程式。
下表为长式周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)表中属于d区的元素是(填编号)。 (2)科学发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如右图(图中②、④、⑨分别位于晶胞的
(2)科学发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如右图(图中②、④、⑨分别位于晶胞的
体心、顶点、面心),则该化合物的化学式为
(用对应的元素符号表示)。
(3)元素②的一种氢化物是重要的化工原料,
常把该氢化物的产量作为衡量石油化工发展水
平的标志。有关该氢化物分子的说法正确的是。
A.分子中含有氢键 B.属于非极性分子
C.含有4个σ键和1个π键 D.该氢化物分子中,②原子采用sp2杂化
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为;该元素与元素①形成的分子X构形为;X在①与③形成的分子Y中的溶解度很大,其主要原因是。
(5)下表为原子序数依次增大的短周期元素A~F的第一到第五电离能数据。
请回答:表中的金属元素是(填字母),其中化合价为+3价的是(填字母);若A、B、C依次为同周期相邻元素,表中显示B比A和C的第一电离能都略大,其原因是
。
某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此兴趣小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去)。已知:常温下,CO能使一些化合物中的金属离子还原
例如:PdCl2 + CO + H2O=Pd↓+ CO2 +2HCl 。反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。

请回答下列问题:
(1)通常实验室制取CO2气体的离子方程式是,为了使制气装置能“随开随用,随关随停”,上图A处应选用的装置是___(填写 “Ⅰ”、“Ⅱ”或“Ⅲ”)。若要制取干燥、纯净的CO2气体,装置B中应盛放的试剂是溶液,装置C中应盛放的试剂是________。
(2)观察实验装置图可知Na与CO2反应的条件是_____________。检查装置的气密性完好并装入药品后,在点燃酒精喷灯前,必须进行的操作是____________________。待装置______(填写字母)中出现现象时,再点燃酒精喷灯,这步操作的目的是。
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:
①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是。
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是。
(4)请用文字简要说明你判断②中D装置生成固体的成分是钠的正盐或酸式盐的理由。。