钛及其化合物大量应用于航空、造船、电子、化学、医疗器械、电讯器材等各个领域。由钛铁矿(FeTiO3)提取金属钛(海绵钛)的主要工艺流程如下(部分产物省略):
(1)氯化的过程是将二氧化钛、碳粉混合,在高温条件下通入氯气制得TiCl4和一种可燃性气体,该反应的化学方程式为 ;TiCl4在室温下为无色液体,氯化后提纯四氯化钛的方法是过滤、____ 。
(2)还原过程是用过量的镁在高温条件下与TiCl4反应制得海绵钛。写出此反应的化学方程式 。
(3)还原过程必须在1070 K的温度下进行,你认为还应该控制的反应条件是 。
(4)常温下,钛不与水、稀盐酸、稀H2SO4或稀HNO3作用,但易溶于氢氟酸,推测其原因是 。
| A.氢氟酸的酸性比其他酸强 |
| B.氢氟酸的氧化性比其他酸强 |
| C.氢氟酸的还原性比其他酸强 |
| D.钛离子易与氟离子形成可溶性难电离物质 |
(5)上述工艺中,得到的海绵钛中可能含有金属镁,常温下除去该杂质应选用的试剂是稀盐酸或稀硫酸,不选择稀硝酸的原因是__ __;若杂质只有金属镁的某海绵钛样品,去除杂质后质量减少十分之一,则该样品中n(Ti):n(Mg)= 。
偏二甲肼与
是常用的火箭推进剂,二者发生如下化学反应:
(Ⅰ)
(1)反应(Ⅰ)中氧化剂是.
(2)火箭残骸中常现红棕色气体,原因为:
(Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)为(填"吸热"或"放热")反应.
(3)一定温度下,反应(Ⅱ)的焓变为
.现将1
充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是 .若在相同温度下,上述反应改在体积为1
的恒容密闭容器中进行,平衡常数(填"增大""不变"或"减小"),反应3
后
的物质的量为0.6
,则0~3
内的平均反应速率
=
.
(4)
可用氨水吸收生成
.25℃时,将
溶于水,溶液显酸性,原因是(用离子方程式表示).向该溶液滴加
氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将填"正向""不"或"逆向")移动,所滴加氨水的浓度为
.(
的电离平衡常数取Kb=2×10﹣5
)
工业上由黄铜矿(主要成分
)冶炼铜的主要流程如下:
(1)气体A中的大气污染物可选用下列试剂中的吸收.
a.浓
b.稀
c.
溶液 d.氨水
(2)用稀
浸泡熔渣B,取少量所得溶液,滴加
溶液后呈红色,说明溶液中存在(填离子符号),检验溶液中还存在Fe2+的方法是 (注明试剂、现象).
(3)由泡铜冶炼粗铜的化学反应方程式为 .
(4)以
溶液为电解质溶液进行粗铜(含
、
、
、
、
等杂质)的电解精炼,下列说法正确的是.
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中
向阳极移动
d.利用阳极泥可回收
、
、
等金属
(5)利用反应
可制备
,若将该反应设计为原电池,其正极电极反应式为 .
难溶性杂卤石(
)属于"呆矿",在水中存在如下平衡
⇌
为能充分利用钾资源,用饱和
溶液溶浸杂卤石制备硫酸钾,工艺流程如图1:
(1)滤渣主要成分有和以及未溶杂卤石.
(2)用化学平衡移动原理解释
溶液能溶解杂卤石浸出
的原因:.
(3)"除杂"环节中,先加入溶液,经搅拌等操作后,过滤,再加入溶液调滤液
至中性.
(4)不同温度下,
的浸出浓度与溶浸时间的关系是图2,由图可得,随着温度升高,①②;

(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生: 已知298 时, =2.80×10﹣9, =4.90×10﹣5,求此温度下该反应的平衡常数 (计算结果保留三位有效数字).
过渡金属催化的新型碳﹣碳偶联反应是近年来有机合成的研究热点之一,如:
反应①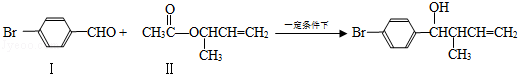
化合物Ⅱ可由化合物Ⅲ合成: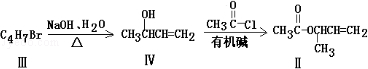
(1)化合物Ⅰ的分子式
(2)化合物Ⅱ与
加成的产物的结构简式为
(3)化合物Ⅲ的结构简式为
(4)在浓硫酸存在和加热条件下,化合物Ⅳ易发生消去反应生成不含甲基的产物,该反应的方程式为(注明反应条件),因此,在碱性条件下,由Ⅳ与
反应生成Ⅱ,其反应类型为.
(5)Ⅳ的一种同分异构体Ⅴ能发生银镜反应,Ⅴ与Ⅱ也可以发生类似反应①的反应,生成化合物Ⅵ,Ⅵ的结构简式为(写出其中一种).
化合物
(
)在氢氧化钠溶液中加热反应后再酸化可得到化合物
和
.回答下列问题:
(1)
的分子式为
,分子中只有一个官能团.则
的结构简式是,
与乙醇在浓硫酸催化下加热反应生成
,该反应的化学方程式是,该反应的类型是;写出两种能发生银镜反应的B的同分异构体的结构简式.
(2)
是芳香化合物,相对分子质量为180,其碳的质量分数为60.0
,氢的质量分数为4.4
,其余为氧,则
的分子式是.
(3)已知
的芳环上有三个取代基,其中一个取代基无支链,且还有能使溴的四氯化碳溶液褪色的官能团及能与碳酸氢钠溶液反应放出气体的官能团,则该取代基上的官能团名称是.另外两个取代基相同,分别位于该取代基的邻位和对位,则
的结构简式是.
(4)
的结构简式是.