常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaC1、MgC12等。请回答
(1)冰比硫化氢熔点高的原因是 ;
其分子中氧原子的杂化轨道类型为 ;
(2)已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
| 电离能/kJ·mol—1 |
I1 |
I2 |
I3 |
I4 |
| X |
578 |
1817 |
2745 |
11578 |
| Y |
738 |
1451 |
7733 |
10540 |
| Z |
496 |
4562 |
6912 |
9543 |
则X、Y、Z的电负性从大到小的顺序为 (用元素符号表示);
(3)融雪剂对环境危害很大,如和路基上的铁等金属形成原电池,会加快路面破损。铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其配离子结构如图。
①铁元素基态原子价电子排布式为 ;
②已知CN—与N1结构相似,1mol CN-中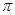 键数目为 。
键数目为 。
写出下列反应的离子方程式:
(1) 铝和氢氧化钾溶液反应___;
(2) 硫酸铝和氨水的反应________;
(3)二氧化硅和氢氧化钠溶液反应____;
现有含NH4+、H+、Al3+、Mg2+、Cl-的溶液100mL,往其中逐滴加入2mol/L的氢氧化钠溶液,并不断搅拌,所得沉淀质量与所加氢氧化钠溶液体积的关系如下图,其中OA段无气体产生,回答下列问题。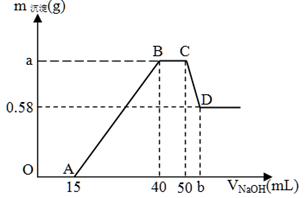
(1)写出下列过程发生反应的离子方程式。
OA段:;
CD段:;
(2)氢氧化镁沉淀的质量m[Mg(OH)2] = g。
(3)a = ;b = 。
(4)原溶液中c(NH4+) = ;c(Cl-) = 。
A、B、C、D、E五种短周期主族元素,原子序数依次增大。A原子的核外电子数等于最外层电子数;B原子的最外层电子数是次外层电子数的2倍;C原子的M层电子数与L层电子数相差7;D原子的最外层电子数是A、B、C三原子的最外层电子数之和。回答下列问题。
(1)元素B在周期表中的位置为第周期族;元素D简单离子的结构示意图为。
(2)元素C、D简单离子的半径由大到小的顺序为(用离子符号表示)。
(3)元素B可形成离子BH3-,下列与其具有相同电子数和质子数的微粒是。
A.NH4+ B.OH- C.F- D.HS-
(4)元素A、C组成化合物甲CA,甲能与水反应产生一种强碱和一种气体,该反应的化学方程式为。
(5)A元素有aA、a+1A、a+2A三种同位素,E元素有eE、e+2E两种同位素,二者所形成分子的相对分子质量有种。
乙酸苯甲酯具有类似茉莉花香的气味,主要用作茉莉、白兰、玉瓒、月下香等的调和香料,由于对花香型和幻想型香精的香韵均有提长作用,且价格低廉,因此在多种香精中有广泛的应用,乙酸苯甲酯可用以下的设计方案合成:
(1)写出A、C的结构简式
A.________________,C.________________.
(2)D有很多种同分异构体,除自身外,含有酯基,且只有一个取代基的同分异构体有五种,其中三种结构简式为
请写出另外二种同分异构体的结构简式:____________________、_____________________.
二甲苯苯环上的一溴代物有六种同分异构体,这些一溴代物与生成它的对应二甲苯的熔点分别是:
| 一溴代二甲苯(℃) |
234 |
206 |
231.8 |
204 |
205 |
214.5 |
| 对应的二甲苯(℃) |
13 |
-54 |
-27 |
-54 |
-54 |
-27 |
由上述数据可推断,熔点为234℃的一溴二甲苯的结构简式是____________,熔点为-54℃的二甲苯的名称是__________________.