A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A是地壳中含量最高的元素,B、C、D同周期,E和其他元素既不在同周期也不在同主族,D的氢化物和最高价氧化物的水化物均为强酸,且B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。据此回答下列问题:
(1)A和D的氢化物中,沸点较高的是 __________(写出化学式)。
(2)写出A单质的结构式___________。B的最高价氧化物的水化物的电子式__________。
(3)写出E离子的离子结构示意图___________________。元素D在元素周期表中的位置是____________________。
(4)A、D、E可以形成多种盐,其中一种盐中A、D、E三种元素的原子个数比为2:2:1,该盐的名称为 __________。它的水溶液与D的氢化物的水溶液反应可生成D的单质,该离子方程式为______________________。
(15分)已知:①A从石油中获得是目前工业上生产的主要途径,A的产量通常用来衡量一个国家的石油化工发展水平;② 。现以A为主要原料合成乙酸乙酯,合成路线如图。
。现以A为主要原料合成乙酸乙酯,合成路线如图。
(1)写出A的结构式__________________。
(2)B、D分子中的官能团名称分别是_____________、______________。
(3)写出下列反应的化学方程式:
①____________________________________;
②____________________________________;
④____________________________________;
(4)下列描述能说明反应④已达到化学平衡状态的有。 ①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②正反应的速率与逆反应的速率相等
③ 单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
④混合物中各物质的浓度不再变化 ⑤单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
⑤单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
(5)反应④制得的乙酸乙酯粗产品中含有少量乙酸、乙醇和水,现拟分离乙酸乙酯、乙酸和乙醇,某小组设计了如下分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。
试剂a是______________,试剂b是_________;分离方法①③分别是_______、________。
下表是元素周期表的一部分,针对表中的①~⑨种元素,用化学用语填空:
(1)元素②的原子结构示意图为___________,元素②原子核内含有6个中子的原子可表示为________。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是__________。
(3)元素①与⑥形成的化合物的电子式为:_______________。
(4)⑤、⑥、⑨三种元素形成的简单离子,离子半径由大到小的顺序是_______________。
(5)实验室用元素③的氢化物制取③的单质的反应为______________________________。
金属冶炼和处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是。
| A.Fe2O3 | B.NaCl | C.Cu2S | D.Al2O3 |
(2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2=4CuSO4+2 H2O,该反应的还原剂是,当1mol O2发生反应时,还原剂所失电子的物质的量为mol。
(3)下图为电解精炼银的示意图,(填a或b)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成的该气体为,电极反应为 。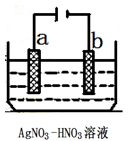
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。回答下列问题: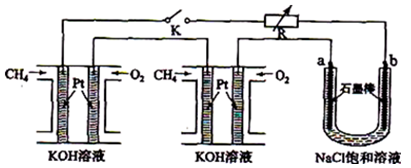
(1)甲烷燃料电池正极、负极的电极反应分别为、。
(2)闭合K开关后,a电极名称是 ,电极方程式为 。
(3)若标准状况下,每个燃料电池中通入1.12L甲烷气体完全反应,则电解池中产生氯气体积为L。
现有A、B、C、D、E、F六种有机物,它们的转化关系如下图所示(图中部分反应条件及生成物没有全部写出)。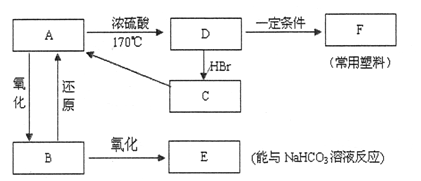
已知:液体B能发生银镜反应,气体D是一种植物生长调节剂,其相对分子质量为28。
请回答下列问题:
(1)B的结构简式,D、E官能团名称分别是、;
(2)D→A的化学方程式是;
(3)D→F反应的化学方程式是;
(4)在一定的条件下,A与E反应可生成一种具有香味的物质。该反应的化学方程式是。