在25℃、1.01×105Pa下,将22 g CO2通入1 mol·L-1NaOH溶液750mL中充分反应,测得反应放出x kJ热量。在该条件上,1 mol CO2通入2 mol·L-1NaOH溶液1 L中充分反应放出y kJ热量。则CO2与NaOH溶液反应生成NaHCO3的热化学方程式是
| A.CO2(g)+NaOH(aq) ="==" NaHCO3(aq);△H=-(4x-y) kJ·mol-1 |
| B.CO2(g)+NaOH(aq) ="==" NaHCO3(aq);△H=-(2x-y) kJ·mol-1 |
| C.CO2(g)+NaOH(aq) ="==" NaHCO3(aq);△H=-(2y-x) kJ·mol-1 |
| D.2CO2(g)+NaOH(1) ="==" NaHCO3(1);△H=-(8x-2y) kJ·mol-1 |
维生素C的结构简式为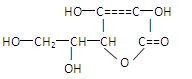 有关它的叙述错误的是
有关它的叙述错误的是
| A.是一种环状的酯类化合物 | B.易起氧化及加成反应 |
| C.可以溶于H2O | D.在碱性溶液中能稳定存在 |
某酯的结构可表示为CmH2m+1COOCnH2n+1,已知m+n=5,该酯的一种水解产物经过催化氧化可转化为它的另一种水解产物,则原来的酯是()
A 、丙酸异丙酯 B、乙酸丁酯 C、丁酸甲酯 D、丙酸丙酯
、丙酸异丙酯 B、乙酸丁酯 C、丁酸甲酯 D、丙酸丙酯
2001年9月1日开始执行的国家食品卫生标准规定,酱油中3—氯丙醇含量不得超过1PPm。相对分子质量为94.5的氯丙醇(不含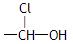 结构)共有
结构)共有
| A.2种 | B.3种 | C.4种 | D.5种 |
有下列物质:①乙醇②苯酚③乙醛④丙烯酸(CH2=CH—COOH)⑤乙酸乙酯,其中与溴水、酸性KMnO4溶液、NaHCO3溶液都能反应的是
A.仅①③ |
B.仅②⑤ | C.仅④ | D.仅③④ |
有机物 在不同条件下至少可能发生7种不同类型的反应:①取代②加成③消去④氧化⑤酯化⑥加聚⑦缩聚。其中由于其分子结构中含有—OH而可能发生的反应有
在不同条件下至少可能发生7种不同类型的反应:①取代②加成③消去④氧化⑤酯化⑥加聚⑦缩聚。其中由于其分子结构中含有—OH而可能发生的反应有
| A.②④⑥⑦ | B.③④⑤⑥ | C.②③④⑤ | D.①③④⑤⑦ |