某一反应物的浓度是1.0mol/L,经过20s后,它的浓度变成了0.2mol/L,在这20s内它的反应速率为
| A.0.04 | B.0.04mol / (L·s) | C.0.08mol(L·s) | D.0.04mol / L |
水溶液中能大量共存的一组离子是
| A.Na+、Al3+、Cl-、CO32- | B.H+、Na+、Fe2+、MnO4- |
| C.K+、Ca2+、Cl-、NO3- | D.K+、NH4+、OH-、SO42- |
某钠盐溶液中可能含有NO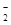 、SO42-、SO32、
、SO42-、SO32、 、Cl-、I-等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
、Cl-、I-等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液的pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体
④加足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色
⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)2溶液,再滴加KSCN溶液,显红色
该同学最终确定在上述六种离子中仅含有NO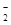 、
、 、Cl-三种阴离子.
、Cl-三种阴离子.
请分析,该同学只需要完成上述哪几个实验,即可得出此结论.( )
| A.①②④⑤ | B.③④ |
| C.③④⑤ | D.②③⑤ |
下列各组离子在指定溶液中一定能大量共存的是( )
| A.在能使石蕊试纸变蓝色的溶液中:Na+、AlO2-、S2-、SO42- |
B.由水电离出的c(H+)=10-12mol·L-1的溶液中:Cl-、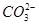 、NH4+、SO32 、NH4+、SO32 |
C.在加入铝粉能产生H2的溶液中:NH4+、Na+、Fe2+、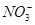 |
| D.pH=2的溶液中:Na+、SO42-、ClO-、SO32 |
下列离子方程式错误的是()
| A.向FeBr2溶液中通入少量的Cl2 2Fe2+ + Cl2 = 2Fe3+ + 2Cl- |
| B.向FeBr2溶液中通入与FeBr2等物质的量的Cl2 2Fe2+ + 2Br- + 2Cl2 = 2Fe3+ + Br2 + 4Cl- |
| C.向FeBr2溶液中通入足量的Cl2 2Fe2+ + 4Br- + 3Cl2 = 2Fe3+ + 2Br2 + 6Cl- |
| D.向苯酚钠溶液中通入“少量”的CO2 |
2 -O-+CO2+H2O→2
-O-+CO2+H2O→2 -OH↓+CO32-
-OH↓+CO32-
下列说法正确的是 ( )
| A.HR溶液导电性较弱,HR属于弱电解质 |
| B.某化合物溶解于水导电,则该化合物为电解质 |
| C.根据电解质在其水溶液中能否完全电离,将电解质分成强电解质与弱电解质 |
| D.食盐是电解质,食盐的水溶液也是电解质 |