(6分)(1)甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ:CH4(g)+H2O(g) CO(g)+3H2(g)ΔH="+206.0" kJ·mol-1
CO(g)+3H2(g)ΔH="+206.0" kJ·mol-1
Ⅱ:CO(g)+2H2(g) CH3OH(g)ΔH="-129.0" kJ·mol-1
CH3OH(g)ΔH="-129.0" kJ·mol-1
CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为 _____________。
(2)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+ 氧化成Co3+,然后以Co3+ 作氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置模拟上述过程:
①写出阳极电极反应式 _______ 。
②写出Co3+除去甲醇的离子方程式 。
某强氧化剂 被亚硫酸钠还原到较低价态,如果还原24个
被亚硫酸钠还原到较低价态,如果还原24个 到较低价态,需要用含60个
到较低价态,需要用含60个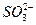 的溶液,那么X元素的最终价态为___________。
的溶液,那么X元素的最终价态为___________。
在下列两个反应中被氧化的氯元素与被还原的氯元素的质量之比各为多少?
(1)2Cl2+2Ca(OH)2====CaCl2+Ca(ClO)2+2H2O
(2)3Cl2+6KOH 5KCl+KClO3+3H2O
5KCl+KClO3+3H2O
在S2-、Fe2+、Mg2+、S、I-、H+、Fe3+中,只有氧化性的是_________;只有还原性的是_________;既有氧化性又有还原性的是_________。
(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
___________+___________ ___________+___________+___________+H2O
___________+___________+___________+H2O
(2)反应物中发生氧化反应的物质是___________,被还原的元素是___________。
(3)反应中1 mol氧化剂___________(填“得到”或“失去”) ___________mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中: ___________+
___________+ ___________
___________
新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。转化流程如图所示:
(1)已知铁酸盐(MFe2O4)被H2高温还原时,发生反应的MFe2O4与H2的物质的量之比为2∶1,则还原产物MFe2Ox中x=________,MFe2Ox中+2价铁与+3价铁的物质的量之比为________。
(2)在酸性溶液中,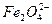 易转化为Fe2+:
易转化为Fe2+: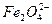 +2e-+8H+====2Fe2++4H2O,有KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种能使上述还原过程发生,写出该氧化还原反应的离子方程式:_____________________________________。
+2e-+8H+====2Fe2++4H2O,有KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种能使上述还原过程发生,写出该氧化还原反应的离子方程式:_____________________________________。