下列说法正确的是
| A.石油的分馏和煤的气化都是发生了化学变化 |
| B.纤维素、油脂和蛋白质在一定条件下都能水解 |
| C.二氧化硅是半导体材料,可将太阳能直接转化为电能 |
| D.乙烯和苯都能使酸性KMnO4溶液褪色 |
铁、铜混合粉末18.0 g 加入到100 mL 5.0 mol/LFeCl3溶液中,剩余固体质量为3.2 g。下列说法正确的是
| A.剩余固体是铁、铜混合物 |
| B.原固体混合物中铜的质量是9.6 g |
| C.反应后溶液中n(Fe3+)="0.10" mol |
| D.反应后溶液中n(Fe2+)+ n(Cu2+)="0.5" mol |
海水开发利用的部分过程如图所示。下列说法错误的是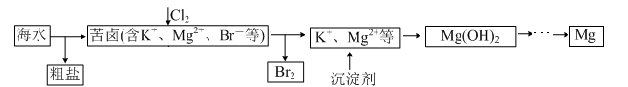
| A.粗盐可采用除杂和重结晶等过程提纯 |
| B.向苦卤中通入Cl2是为了提取溴 |
| C.实际生产中常选用Ca(OH)2 作为沉淀剂 |
| D.工业生产中电解熔融氧化镁的方法制取镁 |
室温下向10 mL 0.1 mol/L NaOH 溶液中加入0.1 mol/L 的一元酸HA 溶液pH 的变化曲线如图所示。下列说法正确的是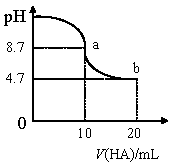
A.a 点所示溶液中c(A-)+c(HA)= 0.1mol/L
B.a、b 两点所示溶液中水的电离程度不同
C.pH="7" 时,c(Na+)=c(A-)+c(HA)
D.b 点所示溶液中c(HA) >c(A-)
在一定温度下,有以下反应:2A(g)+ B(g) 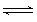 C(g)+D(g) △H<0 ,反应进行至第10 min 时,改变一个条件,当反应进行至第20 min 时,发现生成C的速率增大,C的百分含量也增大,则改变的条件可能是
C(g)+D(g) △H<0 ,反应进行至第10 min 时,改变一个条件,当反应进行至第20 min 时,发现生成C的速率增大,C的百分含量也增大,则改变的条件可能是
| A.加热 | B.使用催化剂 | C.加压 | D.分离出D |
某有机物的结构简式如图所示,有关该有机物的叙述正确的是
| A.分子中含有3 种官能团 |
| B.在一定条件下,能发生取代、氧化、酯化和加聚反应 |
| C.该物质分子中最多可以有10 个碳原子在同一平面上 |
| D.1 mol 该物质最多可与5 mol H2 发生加成反应 |