已知甲、乙、丙三种物质均含有同一种中学常见元素X,其转化关系如下: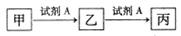
下列说法不正确的是
| A.若乙为NaHCO3,则丙一定是CO2 |
| B.若A为氯水,X为金属元素,则甲与丙反应可生成乙 |
| C.若A为NaOH溶液,X为短周期的金属元素,则乙一定为白色沉淀 |
| D.若甲为单质硫,则丙溶于水形成的浓溶液能与碳反应可生成乙 |
光纤通讯是70年代后期发展起来的一种新型通信技术,目前长距离光纤通讯系统已经投入使用。光纤通讯的光学纤维是由下列哪种物质经特殊工艺制成()
| A.石墨 | B.二氧化硅 | C.氧化镁 | D.氧化铝 |
“垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅、铝制的易拉罐、铜导线等可以归为一类加以回收,它们属于()
| A.氧化物 | B.盐 | C.金属或合金 | D.碱 |
对分子量为104的烃的下列说法,正确的组合是()
①可能是芳香烃②可能发生加聚反应
③分子中不可能都是单键④分子中可能都是单键
| A.只有①② | B.只有①③ | C.只有①②③ | D.只有①②④ |
 都属于萘(结构简式:
都属于萘(结构简式: )的同系物。则萘和萘的同系物分子组成通式是()
)的同系物。则萘和萘的同系物分子组成通式是()
| A.CnH2n-6(n≥6) | B.CnH2n-8(n≥10) | C.CnH2n-10(n≥10) | D.CnH2n-12(n≥10) |
用一种试剂就能区分开苯酚、乙醇、NaOH溶液、AgNO3溶液、KSCN溶液这六种无色液体。它是()
| A.溴水 | B.FeCl3溶液 | C.金属钠 | D.CuO |