(14分)乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化为烃B、烃C。以C为原料可以合成聚对羟基苯甲酸 (G)。已知:
(1)A是一种有机酸,分子式为C9H10O3。
(2)B的相对分子质量为104,分子中含苯环且能使溴的四氯化碳溶液褪色。
(3)C的相对分子质量为78,且分子中只有一种氢原子。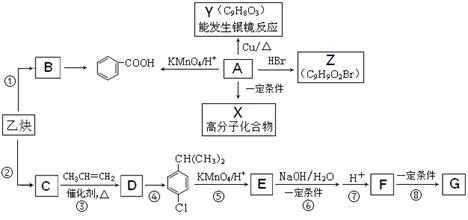
(1)写出乙炔分子的电子式_________, F中的含氧官能团名称_____________;
(2)上述①至⑧的反应中,属于加成反应的有____________,
第④步反应所需的试剂和条件是_____________;
(3)写出A的结构简式_________________;
(4)下列有关的描述中,正确的是__________;
a.1molB最多能与4molH2加成
b.B通过氧化反应可使溴水和酸性KMnO4溶液褪色
c.B、C、D是同系物
d.A→X的反应属于缩聚反应
(5)写出F→G反应的化学方程式___________________________________。
【化学—选修2:物质结构与性质】A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是________(填元素符号),其中C原子的核外电子排布式为________;
(2)单质A有两种同素异形体,其中沸点高的是________(填分子式),原因是________;A和B的氢化物所属的晶体类型分别为______和_______;
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为________,中心原子的杂化轨道类型_______;
(4)化合物D2A的立体构型为________,中心原子的价层电子对数为________,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为_______;
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566nm,F的化学式为________,晶胞中A原子的配位数为_______;列式计算晶体F的密度_______。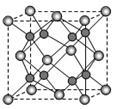
酸牛奶是人们喜爱的一种营养饮料。酸牛奶中有乳酸菌可产生乳酸等有机酸,使酸碱度降低,有效地抑制肠道内病菌的繁殖。酸牛奶中的乳酸可增进食欲,促进胃液分泌,增强肠胃的消化功能,对人体具有长寿和保健作用,乳酸的结构为: 。工业上它可由乙烯来合成,方法如下:
。工业上它可由乙烯来合成,方法如下: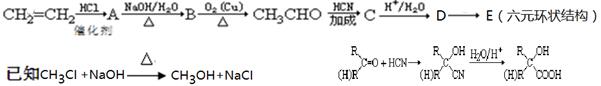
(1)D的结构简式 ,所含的官能团的名称是 。
(2)写出下列转化的化学方程式:
①A的生成 。
②C的生成 。
③B的生成 。
④D→E 。
菠萝酯F是一种具有菠萝香味的赋香剂,其合成路线如下: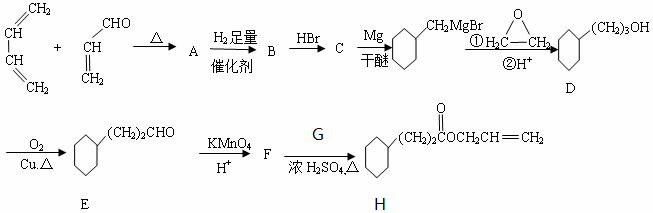
已知:
(1)A的结构简式为 , G物质核磁共振氢谱共有 个峰。
(2)写出F和G反应生成H的化学方程式 。写出D生成E的化学方程式 。
(3)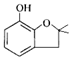 呋喃酚是一种合成农药的重要中间体,它的同分异构体很多,写出符合下列条件的所有芳香族同分异构体的结构简式: 。
呋喃酚是一种合成农药的重要中间体,它的同分异构体很多,写出符合下列条件的所有芳香族同分异构体的结构简式: 。
①环上的一氯代物只有一种 ②含有酯基 ③能发生银镜反应
(4)结合题给信息,以溴乙烷和环氧乙烷为原料制备1-丁醇,设计合成路线(其他试剂任选)。合成路线流程图示例: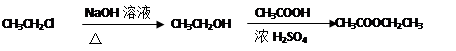
合成路线:________________________________________
一种重要的有机化工原料有机物X,下面是以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。Y是一种功能高分子材料。
已知:
①X为芳香烃,其相对分子质量为92
②烷基苯在高锰酸钾的作用下,侧链被氧化成羧基:
③ (苯胺,易被氧化)
(苯胺,易被氧化)
请根据本题所给信息与所学知识回答下列问题:
(1)X的分子式为______________,其侧链氢原子全部被苯环取代后,最多有 个碳原子共面;(2) 的名称为____________________,G中官能团名称为___________;
的名称为____________________,G中官能团名称为___________;
(3)反应③的反应类型是________;已知A为一氯代物,则E的结构简式是____________;(4)反应④的化学方程式为__________________________________________;
(5)阿司匹林有多种同分异构体,满足下列条件的同分异构体有________种:
①含有苯环;
②既不能发生水解反应,也不能发生银镜反应;
③1 mol该有机物能与2 molNaHCO3完全反应。
(6)参照上述合成路线,结合所学知识,设计一条以A为原料制备 的合成路线(无机试剂任用)。合成路线流程图示例如下:
的合成路线(无机试剂任用)。合成路线流程图示例如下: 。
。
有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阴离子且互不重复)。
| 阳离子 |
Na+、Ba2+、NH4+ |
| 阴离子 |
CH3COO-、Cl-、OH-、SO42- |
已知:①A、C溶液的pH均大于7,A、B的溶液中水的电离程度相同;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象。
(1)A是__________。
(2)25 ℃时,0.1 mol·L-1 B溶液的pH=a,则B溶液中c(H+)-c(NH3·H2O)=________(用含有a的关系式表示)。
(3)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为____________________________________。
(4)在一定体积的0.005 mol·L-1的C溶液中,加入一定体积的0.001 25 mol·L-1的盐酸时,混合溶液的pH=11,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是________。