下列说法正确的是
| A.在“研究反应速率的影响因素”实验中:Na2S2O3+H2SO4=Na2SO4+S+SO2+H2O,可通过观察产生气泡的快慢来比较不同条件下该反应的速率大小 |
| B.为了精确测定盐酸与氢氧化钠溶液反应的反应热,当两者混合后,立即读取温度计的读数,防止热量散失 |
| C.将铁粉、碳粉、少量氯化钠和水混合放在塑料袋中搓揉,用手触摸会感觉到发热,袋里产生大量铁锈 |
| D.酸碱中和滴定实验中,终点判断过迟,导致标准液滴多,只能重新滴定 |
百里酚酞是常用的滴定指示剂,pH小于9.4为无色,大于10.6时为蓝色,百里酚酞的结构式如右图,可由邻苯二甲酸酐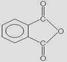 等原料合成得到。有关说法不正确的是
等原料合成得到。有关说法不正确的是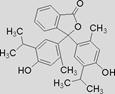
| A.百里酚酞中含有羟基、酯基及苯基等官能团 |
| B.邻苯二甲酸酐分子中所有原子处于同一平面 |
| C.1mol百里酚酞在溶液中最多可与4molNaOH反应 |
| D.用已知浓度的烧碱滴定未知浓度的盐酸,用酚酞作指示剂比百里酚酞误差小 |
镁/H2O2酸性燃料电池采用海水作电解质(加入一定量的酸),下列说法不正确的是
| A.电池总反应为:Mg+H2O2=Mg(OH)2 |
| B.正极发生的电极反应为:H2O2+2H++2e-=2H2O |
| C.工作时,正极周围海水的pH增大 |
| D.电池工作时,溶液中的H+向负极移动 |
下列离子方程式书写正确的是
| A.氨水吸收少量的二氧化硫:NH3·H2O + SO2 = NH4+ + HSO3- |
B.用两个铜片作电极电解盐酸:Cu + 2H+  H2↑+ Cu2+ H2↑+ Cu2+ |
| C.钠与水反应:Na +2H2O = Na+ +2OH- +H2↑ |
| D.铜与稀硝酸反应:3Cu +8H+ + 2NO3- = 3Cu2+ +2NO↑ +4H2O |
2008年北京奥运会主体育场——“鸟巢”,被《泰晤士报》评为全球 “最强悍”工程。 “鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料。有关说法正确的是
| A.合金的熔点通常比组分金属高,硬度比组分金属小 |
| B.已知Ga处于ⅢA主族,可推知氮化镓化学式为Ga3N2 |
| C.用金属铝与V2O5冶炼钒,铝作还原剂 |
D.ETFE膜(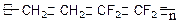 )是由两种单体缩聚而成的 )是由两种单体缩聚而成的 |
下列有关生活中的化学问题,说法正确的是
| A.因脂肪氧化产生的能量比糖类高,可大量饮食脂肪 |
| B.若工厂贮氯罐意外泄漏时,应紧急组织邻近群众沿逆风方向撤离 |
| C.人体中不含水解纤维素的酶,故人类饮食中不需摄入纤维素含量高的食品 |
| D.给酸性土壤施肥时,可将铵盐与石灰混合后再使用 |