反应:X(g)+3Y(g)  2Z(g) △H<0达平衡后,将气体混合物的温度降低,下列叙述中正确的是
2Z(g) △H<0达平衡后,将气体混合物的温度降低,下列叙述中正确的是
| A.正反应速率加大,逆反应速率变小,平衡正向移动 |
| B.正反应速率变小,逆反应速率加大,平衡逆向移动 |
| C.正反应速率和逆反应速率都变小,平衡正向移动 |
| D.正反应速率和逆反应速率都变小,平衡逆向移动 |
将含有0.400molCuSO4和0.200molKCl的水溶液1L,用惰性电极电解一段时间后,在一个电极上析出19.2gCu,此时在另一电极上放出的气体在标准状况下的体积为
| A.5.60L | B.6.72L | C.4.48L | D.3.36L |
一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍。电池总反应为:C2H5OH +3O2=2CO2 +3H2O,电池示意图如下图。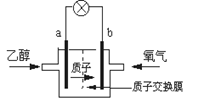
下面对这种电池的说法正确的是
| A.b极为电池的负极 |
| B.设每个电子所带电量为q库仑,则1mol乙醇被氧化产生12NAq库仑的电量 |
| C.电池工作时电流由a极沿导线经灯泡再到b极 |
| D.电池正极的电极反应为: O2+4e-+2H2O=4OH- |
用惰性电极电解一定量的硫酸铜溶液,实验装置如图甲,电解过程中的实验数据如图乙。横坐标表示转移电子的物质的量,纵坐标表示产生气体的总体积(标准状况)。则下列说法不正确的是
| A.电解过程中,a电极表面先有红色物质析出,后有气泡产生 |
| B.b电极上发生的反应方程式为:4OH--4e- =2H2O+O2↑ |
| C.从开始到Q点时收集到的混合气体的平均摩尔质量为12 g/ mol |
| D.从开始到P点收集到的气体是O2 |
将足量的CO2不断通入KOH、Ba(OH)2、KA1O2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为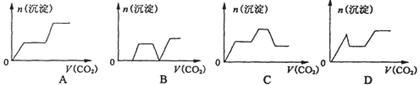
在下图点滴板上有四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是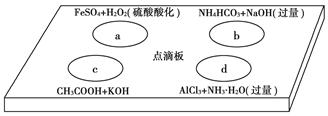
| A.a反应:Fe2++2H++H2O2===Fe3++2H2O |
| B.b反应:HCO3-+OH-===CO23-+H2O |
| C.c反应:H++OH-===H2O |
| D.d反应:Al3++3NH3·H2O===Al(OH)3↓+3NH4+ |