某地方政府为了实现对当地水资源及沿途流域环境的综合治理,引导甲、乙两个相邻的工厂在污水处理方面做了横向联合。已知两厂排放的污水经初步处理后,分别只有下列8种离子中的4种(两厂不含相同离子):Ag+、Ba2+、Fe3+、Na+、Cl-、SO42-、NO3-、OH-。两厂单独排放都会造成严重的水污染,如将两厂的污水按一定的比例混合,沉淀后污水便变成无色澄清的只含硝酸钠的水而排放,污染程度会大大降低。关于污染源的分析,你认为正确的是
| A.SO42-和NO3-可能来自同一工厂 | B.Cl-和NO3-一定来自不同的工厂 |
| C.Ag+和Na+可能来自同一工厂 | D.Na+和NO3-来自同一工厂 |
下列有机物或有机物组合,在现有条件下不能发生聚合反应的是( )
D.(CH3)2C(CH3)2
下列事实:①甲苯能使KMnO4(H+)溶液褪色而乙烷不能;②甲醛能发生银镜反应而甲醇不能;③苯酚分子中的羟基酸性比乙醇分子中的羟基酸性强。可以说明有机物分子中的原子间(或原子与原子团之间)的相互影响会导致物质化学性质不同的是( )
| A.只有①③ | B.只有①② | C.只有②③ | D.①②③ |
一定温度下,W g下列物质在足量氧气中充分燃烧,产物与过量的Na2O2完全反应,Na2O2固体增重W g,符合此要求的组合是( )
①H2 ②CO ③CO和H2 ④HCOOCH3⑤HOOC—COOH
| A.全部 | B.仅④⑤ | C.仅①②③ | D.除⑤外 |
中草药素皮中含有的七叶树内酯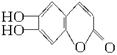 (碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别是( )
(碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别是( )
| A.3 mol,2 mol | B.3 mol,4 mol | C.2 mol,3 mol | D.4 mol,4 mol |
分别将下列各组物质等体积混合,在室温下激烈振荡,静置后,能够分层的是( )
| A.甲醛、水 | B.乙醇、水 | C.乙酸乙酯、水 | D.甘油、水 |